Методическая разработка урока химии для 8 класса.
Автор: Владимирская Л.В., учитель химии МАОУ «Лицей №5» г. Перми.
Класс 8 класс. Тема: «Основания».
Тип урока: урок открытия новых знаний.
Цель: сформировать представление о классе сложных веществ – основаниях, их составе, общей формуле и их названиях, классификации оснований, рассмотреть качественные реакции растворимых в воде оснований.
Задачи:
- образовательные: сформировать знания учащихся о новом классе неорганических веществ - основаниях.
- развивающие: выработать умения определять принадлежность веществ к классу оснований, умение называть их, составлять формулы и пользоваться таблицей растворимости кислот, оснований и солей в воде для определения растворимости оснований; развивать логику, умение выражать свои мысли, анализировать, обобщать факты.
- воспитательные: осознанно достигать поставленной цели; воспитывать положительное отношение к совместному труду.
Ход урока 1. Организационный момент.
2. Проверка знаний.
Проверочная работа по оксидам (приложение № 1)
3. Изучение нового материала.
1. Актуализация знаний и выход на тему урока (фронтальная беседа)
- Учащимся предлагается выполнить задание (слайд № 1)
- Почему оставшиеся вещества нельзя отнести к оксидам?
- Знакомы вам эти вещества?
- Тема урока «Основания»
2. Состав, определение и общая формула оснований
- Что общего между этими веществами? (слайд № 3)
- Сформулируйте определение и запишите общую формулу оснований (слайд № 4)
3. Названия оснований (слайд № 5)
- составление формул оснований (слайд № 6-8) (работа в парах)
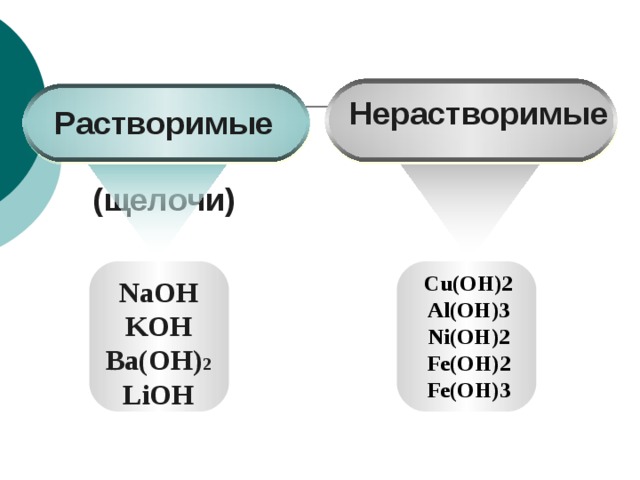
4. Классификация оснований.
- На какие группы можно поделить основания по отношению к воде?
(анализ с использованием таблицы растворимости) (слайд № 9)
- По какому признаку основания разделены на 3 группы? ( слайды № 10,11)
5. Качественное определение щелочей индикаторами
- понятие индикаторы (слайд № 12)
- выполнение лабораторного опыта (приложение № 2)
- окраска индикаторов в щелочной среде (слайд № 13)
4. Закрепление изученного материала
- Крестики –нолики» (слайд № 14)
- Третий лишний. Почему? (слайд № 15)
5. Домашнее задание (слайд № 16)
6. Рефлексия (слайд № 17)
Приложение № 1
Вариант № 1
Из списка веществ выпишите и назовите оксиды металлов: PH3, SiO2, K2O,Na2S,
CuO, CaCl2, CrO, H2O2.
Составьте формулы оксидов: оксид лития, оксид железа (III), оксид серы(VI),
оксид хлора (VII), оксид водорода.
Вариант № 2
Из списка веществ выпишите и назовите оксиды неметаллов: OF2, CaO, H2O,
P2O5, MgO, N2O3, HF, NH3.
Составьте формулы оксидов: оксид марганца(II), оксид алюминия, оксид бария,
оксид углерода(IV), оксид меди(I)
Приложение № 2
Определение щелочной среды (наличие гидроксогруппы)
При работе со щелочами соблюдайте ТБ.
Не допускайте попадания на кожу и одежду
В пробирку налейте 1мл гидроксида натрия и добавьте несколько капель лакмуса. Как изменился цвет раствора?
В пробирку налейте 1мл гидроксида натрия и добавьте несколько капель метилового оранжевого. Как изменился цвет раствора?
В пробирку налейте 1мл гидроксида натрия и добавьте несколько капель фенолфталеина. Как изменился цвет раствора?
Заполните таблицу
| Название индикатора | Окраска индикатора в щелочной среде |
| Лакмус |
|
| Метиловый оранжевый |
|
| Фенолфталеин |
|