
Распределите формулы по классам в таблицу
оксиды
основания
кислоты
K 2 S, P 2 O 5 , NaOH, HCI, CuO,
CuSO 4 , HNO 3 , Ba(OH) 2 , MgO,
H 2 SO 4 , KO Н , BaCI 2 , SO 3 , NaNO 3

Распределите формулы по классам в таблицу
оксиды
основания
P 2 O 5 , CuO, MgO, SO 3 ,
NaOH, Ba(OH) 2 , KO Н ,
кислоты
HCI HNO 3 , H 2 SO 4 ,
K 2 S, P 2 O 5 , NaOH, HCI, CuO,
CuSO 4 , HNO 3 , Ba(OH) 2 , MgO,
H 2 SO 4 , KO Н , BaCI 2 , SO 3 , NaNO 3

Тема

Цели:
- освоить знания о …………………………..
- выработать умения .……………………….
-освоить алгоритм … ………………………….
- вырабатывать умения применять …………………………………….
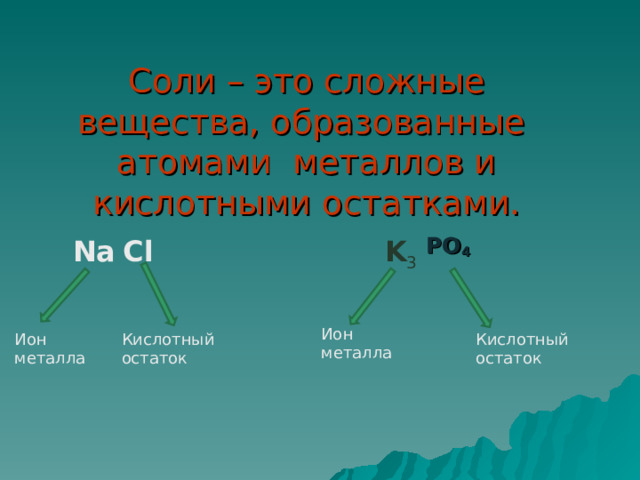
Соли – это сложные вещества, образованные атомами металлов и кислотными остатками.
Na
Cl
K 3
PO 4
Ион
металла
Ион
металла
Кислотный
остаток
Кислотный
остаток

- Cl - хлориды; хлорид калия – KCl
= SO 4 - сульфаты; Сульфат калия – K 2 SO 4 ;
= SO 3 сульфиты, сульфит натрия – Na 2 SO 3
= СО 3 – карбонаты, К 2 СО 3 –карбонат калия
- NO 3 - нитраты, К NO 3 –нитрат калия
≡ РО 4 –ортофосфат, К 3 РО 4 –ортофосфат калия
Формула поваренной соли NaCl

Назовите следующие вещества
СаSO 4_____________________________________
Fe(NO3) 2_____________________________
ВаCl 2_______________________________________
Li 2 SO 3 . ________________________

Составьте формулы солей:
хлорид железа ( III )_____________
нитрат бария__________________
сульфат алюминия_____________.
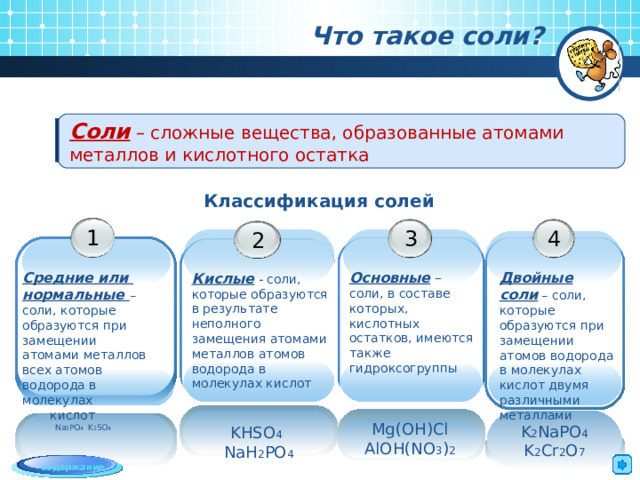
Что такое соли?
Соли – сложные вещества, образованные атомами металлов и кислотного остатка
Классификация солей
1
3
4
2
Средние или
нормальные – соли, которые образуются при замещении атомами металлов всех атомов водорода в молекулах
кислот
Основные – соли, в составе которых, кислотных остатков, имеются также гидроксогруппы
Двойные соли – соли, которые образуются при замещении атомов водорода в молекулах кислот двумя различными металлами
Кислые - соли, которые образуются в результате неполного замещения атомами металлов атомов водорода в молекулах кислот
K 2 NaPO 4
K 2 Cr 2 O 7
KHSO 4
NaH 2 PO 4
Na 3 PO 4 K 2 SO 4
Mg(OH)Cl
AlOH(NO 3 ) 2
содержание

Свойства солей
Физические свойства
Соли - твердые вещества разного цвета.
Растворимость их различна.
Некоторые хорошо растворимы, например все нитраты.
Другие же, например: CaCO 3 , BaSO 4 - практически нерастворимы.
Нитраты – все растворимы
Сульфаты – все, кроме CaSO 4 , SrSO 4 , BaSO 4 , PbSO 4 , Ag 2 SO 4
Хлориды – все, кроме AgCl , PbCl 2
Сульфиды, карбонаты, силикаты, фосфаты – все соли нерастворимые, кроме солей K , Na и групп NH 4
содержание

Химические свойства
- Соли реагируют с металлами ( исключения активные металлы: Li , Na , K , Ca , Ba - которые при обычных условиях реагируют с водой):
Fe + CuSO 4 = FeSO 4 + Cu
- Соли реагируют с кислотами:
Na 2 CO 3 + 2HCl = 2NaCl + CO 2 + H 2 O
- Карбонаты, сульфиты разлагаются при нагревании:
СaCO 3 = CaO + CO 2
- Некоторые соли способны реагировать с водой с образованием кристаллогидратов:
CuSO 4 + 5H 2 O = CuSO 4 5 H 2 O + Q

- Соли реагируют с некоторыми кислотными оксидами:
CaCO 3 + SiO 2 = CaSiO 3 + CO 2
- Соли реагируют с неметаллами, стоящими в ряду, составленным Н. Н. Бекетовым правее, чем неметалл входящий в состав соли:
2NaBr + Cl 2 = 2NaCl + Br 2
- Соли реагируют с другими солями с образованием новых нерастворимых солей:
Na 2 SO 4 + BaCl 2 = BaSO 4 + 2NaCl
- Соли реагируют с растворимыми основаниями с образованием нерастворимого основания:
AlCl 3 + 3KOH = Al(OH) 3 + 3KCl

Получение солей
- Взаимодействие металлов и неметаллов:
2Fe + 3Cl 2 = 2FeCl 3
- Взаимодействие кислотных оксидов с основными и амфотерными оксидами:
CaO + CO 2 = CaCO 3
ZnO + SiO 2 = ZnSiO 3
- Взаимодействие двух разных солей с образованием новой
нерастворимой соли:
Na 2 CO 3 + CaCl 2 = CaCO 3 + 2NaCl
- Взаимодействие оснований и кислот:
NaOH + HCl = NaCl + H 2 O
2Fe(OH) 3 + 3H 2 SO 4 = Fe 2 (SO 4 ) 3 +6H 2 O
Ca(OH) 2 + CO 2 = CaCO 3 + CO 2
- Взаимодействие более активного металла с солями:
FeCl 2 + Zn = ZnCl 2 + Fe
- Действие кислот - неокислителей на металлы, стоящие в ряду напряжений металлов до водорода:
Zn + 2HCl = ZnCl 2 + H 2
содержание

Применение солей
Значение солей для человека
Название солей
Продукты содержания
Соли кальция
Молоко, рыба, овощи
Соли железа
Влияние на человеческий организм
Повышают рост и прочность костей
Яблоки, абрикосы
Соли магния
Заболевания при нехватке солей
Горох, курага
Плохой рост скелета, разрушение зубов
Входят в состав гемоглобина
Малокровие
Улучшают работу кишечника
Ухудшение работы пищеварительной системы

Задачи
В результате реакции с азотной кислотой прореагировало 0,1 моль оксида меди ( II ). Найдите массу и количество вещества нитрата меди ( II) , получившегося в результате реакции
Составьте уравнения реакций, схема которой дана ниже:
CaCO 3 CaO Ca(OH) 2 CaCO 3 Ca(NO 3 ) 2

Решение задачи
Дано: Решение:
n (CuO) = 0 ,1 моль CuO + 2HNO 3 = Cu(NO 3 ) 2 + H 2 O
HNO 3 n = 1 моль n = 1 моль
_________________________
m (Cu(NO 3 ) 2 ) - ? n (CuO) = n (Cu(NO 3 ) 2 = 0,1 моль
n (Cu(NO 3 ) 2 ) - ?
m = n Х M
M (Cu(NO 3 ) 2 = 64 + 2(14 + 3 Х 16) = 188 (г / моль)
m (Cu(NO 3 ) 2 = 0,1 моль Х 188 г / моль = 18,8 (г)
Ответ: масса нитрата меди ( II) равна 18,8 грамм, а его количество вещества – 0,1 моль.

Решение генетической цепочки
- СaCO 3 = CaO + CO 2
- CaO + H 2 O = Ca(OH) 2
- Ca(OH) 2 + CO 2 = CaCO 3 + H 2 O
- CaCO 3 + 2HNO 3 = Ca(NO 3 ) 2 + 2H 2 O


































