Вариант 1.
1. Какая формулировка Периодического закона является современной?
а) Свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины их атомной массы.
б) Свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины зарядов их атомных ядер.
2. Как определяется место химического элемента в периодической системе Д.И. Менделеева?
а) количеством электронов на внешнем уровне
б) количеством нейтронов в ядре
в) зарядом ядра атома
г) атомной массой
3. Как определить число энергетических уровней в атоме элемента?
а) по порядковому номеру элемента
б) по номеру группы
в) по номеру ряда
г) по номеру периода
4. Чем отличаются атомы изотопов одного элемента?
а) числом протонов
б) числом нейтронов
в) числом электронов
г) зарядом ядра
5. Как меняются радиусы атомов в периоде?
а) увеличиваются
б) уменьшаются
в) не изменяются
г) изменяются чуть-чуть
6. Какой элемент возглавляет главную подгруппу пятой группы?
а) ванадий
б) азот
в) фосфор
г) мышьяк
7. Укажите элемент, возглавляющий большой период периодической системы элементов:
а) Cu (№29)
б) Ag (№47)
в) Rb (№37)
г) Au (№79)
8. Элемент, в ядре атома которого содержится 26 протонов:
а) S
б) Cu
в) Fe
г) Ca
9. Чему равно число нейтронов в атоме +15Р31?
а) 31
б)16
в)15
г) 46
10. Чему равно массовое число азота +7N который содержит 8 нейтронов?
а)14
б)15
в)16
г)17
11. Какое число валентных электронов у атома кремния?
а) 1
б) 2
в) 3
г) 4
12. Сколько энергетических уровней у атома скандия?
а) 1
б) 2
в) 3
г) 4
13. Атомы натрия и магния имеют:
а) одинаковое число электронов
б) одинаковое число электронных уровней
в) одинаковую степень окисления в оксидах
г) одинаковое число протонов в ядрах
14. Число неспаренных электронов в атоме алюминия равно:
а) 1
б) 2
в) 3
г) 0
15. Определите какой это элемент 1s22s22p1:
а) №1
б) №3
в) №5
г) №7
16. В соединении калия с хлором химическая связь
а) ковалентная полярная
б) ковалентная неполярная
в) ионная
г) металлическая
17. В соединении калия с кислородом химическая связь
а) металлическая
б) ковалентная полярная
в) ковалентная неполярная
г) ионная
18.Тип связи в молекуле азотной кислоты
а) ковалентная полярная
б) ионная
в) металлическая
г) ковалентная неполярная
19. Химическая связь соответственно: ионная, ковалентная полярная, ковалентная неполярная
а) NaCl, NH3, Br2
б) H2O, CaO, KCl
в) Cl2, MgO, HCl
г) NaOH, H2S, CO
20. Ковалентная неполярная связь в веществе
а) аммиак
б) сероводород
в) хлор
г) железо
21. Молекулярная кристаллическая решетка у
а) оксида серы (VI)
б) магния
в) кислорода
г) хлорида натрия
22. формула вещества с ионной связью
а) K2S
б) NH3
в) O2
г) CaO
23.Формула вещества с ковалентной полярной связью
а) KNO3
б) HNO3
в) Cl2
г) NaCl
24. Ионная кристаллическая решетка у
а) углекислого газа,
б) нитрата натрия,
в) воды,
г) графита
25. Атомная кристаллическая решетка у
а) алмаза
б) поваренной соли
в) аммиака
г) кристаллической соды
26. Наибольшую температуру плавления имеет вещество
а) с ионной кристаллической решеткой
б) с атомной кристаллической решеткой
в) с молекулярной кристаллической решеткой
г) с металлической кристаллической решеткой
27. Схема электронного строения 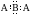 соответствует веществу, формула которого
соответствует веществу, формула которого
а) NH3,
б) СН4,
в) H2S,
г) CaCl2
28. Какое из веществ образовано металлической связью?
а) SO3
б) N2O
в) Br2
г) Fe
29. Вещество, не образованное ионной связью
а) хлорид калия
б) оксид натрия
в) нитрат магния
г) оксид серы (VI)
30. Высокая электропроводность и теплопроводность характерны для веществ с
а) металлической связью
б) ионной связью
в) ковалентной полярной связью
г) ковалентной неполярной связью
Вариант 2.
1.Какую формулировку Периодическому закону дал Д. И. Менделеев?
а) Свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины их атомной массы
б) Свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины заряда их атомных ядер
2. Что показывает номер периода?
а) число валентных электронов
б) число нейтронов
в) число энергетических уровней
г) число электронов на внешнем энергетическом уровне
3.Как изменяются химические свойства элементов в периоде?
а) усиливаются металлические
б) усиливаются неметаллические
в) не изменяются
г) ослабевают неметаллические
4. Ядра атомов изотопов отличаются числом:
а) протонов
б) нейтронов
в) протонов и нейтронов
г) протонов и электронов
5. Как меняются радиусы атомов в главных подгруппах?
а) увеличиваются
б) уменьшаются
в) не изменяются
г) изменяется чуть-чуть
6. Какой элемент возглавляет главную подгруппу шестой группы?
а) ванадий
б) кислород
в) фосфор
г) мышьяк
7.Сколько химических элементов в четвертом периоде:
а)8
б)18
в) 30
г)3 2
8. Элемент, в ядре атома которого содержится 16 протонов:
а) S
б) Cu
в) Fe
г) Ca
9. Число нейтронов в ядре атома 19К39 равно:
а) 19
б) 20
в) 39
г) 58
10.Чему равно массовое число хлора +17Сl, который содержит 20 нейтронов?
а) 37
б)18
в) 20
г)17
11. Какое число валентных электронов у атома кальция?
а) 1
б) 2
в) 8
г) 10
12. Сколько энергетических уровней у атома хрома?
а) 1
б) 2
в) 3
г) 4
13. Атомы углерода и кремния имеют:
а) одинаковое число электронных уровней
б) одинаковые радиусы
в) одинаковое число электронов на внешнем электронном уровне
г) одинаковое число протонов в ядре
14.Число неспаренных электронов в атоме углерода равно:
а) 1
б) 2
в) 3
г) 0
15. Определите какой это элемент 1s22s22p3:
а) №1
б) №3
в) №5
г) №7
16. Какое из указанных веществ образовано ионной связью?
а) NH3
б) К2О
в) H2О
г) СН4
17. Какое из указанных веществ имеет ковалентную неполярную связь?
а) Br2
б) NO2
в) CO
г) NaCl
18. Какое из указанных веществ имеет ковалентную полярную связь?
а) Nа2S
б) N2
в) H2S
г) CaO
19. Тип связи в веществе, формула которого H2CO3
а) ковалентная неполярная
б) ионная
в) металлическая
г) ковалентная полярная
20. Тип связи в веществе, формула которого СuО
а) металлическая
б) ионная
в) ковалентная полярная
г) ковалентная неполярная
21. Тип кристаллической решетки у вещества CaCl2
а) ионная
б) молекулярная
в) атомная
г) металлическая
22. Ковалентная полярная связь характерна для каждого из двух веществ
а) алмаз, хлорид калия
б) кислород, метан
в) сероводород, метан
г) калий, аммиак
23. Ионная связь характерна для каждого из двух веществ
а) магний, хлорид натрия
б) оксид кальция, бромид калия
в) вода, азот
г) калий, аммиак
24. Ковалентная неполярная связь характерна для каждого из двух веществ
а) оксид углерода (II), хлорид калия
б) аммиак, углекислый газ
в) кислород, азот
г) бромид калия, бром
25. Ионная и ковалентная полярная связи соответственно у веществ
а) NaBr, CH4
б) NH3, O2
в) H2O, H2S
г) KCl, Na2O
26. Ковалентная неполярная и ковалентная полярная связи соответственно у веществ
а) O2, NaCl
б) N2, CH4
в) KBr, CO
г) Br2, Cl2
27. Ионная и ковалентная неполярная связи соответственно у веществ
а) NH3, O2
б) СаO, H2O
в) Cl2, H2S
г) MgCl2, Br2
28. В веществе, формула которого FeCl3, тип связи
а) ионная
б) ковалентная полярная
в) ковалентная неполярная
г) металлическая
29. В веществе, формула которого NH4Cl, тип связи
а) ковалентная полярная
б) ионная
в) ковалентная неполярная
г) нет правильного ответа
30. В веществе СН4 химическая связь
а) ионная и ковалентная неполярная
б) ионная и ковалентная полярная
в) ковалентная полярная и ковалентная неполярная
г) металлическая и ковалентная полярная
Карта ответов:
| № | 1 вариант | 2 вариант |
| 1 | б | А |
| 2 | В | В |
| 3 | Г | Б |
| 4 | Б | Б |
| 5 | Б | А |
| 6 | Б | Б |
| 7 | В | Б |
| 8 | В | А |
| 9 | Б | Б |
| 10 | Б | А |
| 11 | Г | Б |
| 12 | Г | Г |
| 13 | Б | В |
| 14 | А | Б |
| 15 | В | Г |
| 16 | В | Б |
| 17 | Г | А |
| 18 | А | В |
| 19 | А | Г |
| 20 | В | Б |
| 21 | В | А |
| 22 | А | В |
| 23 | Б | Б |
| 24 | Б | В |
| 25 | А | А |
| 26 | Б | Б |
| 27 | В | Г |
| 28 | Г | А |
| 29 | Г | Б |
| 30 | А | в |






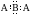 соответствует веществу, формула которого
соответствует веществу, формула которого 









