Тестирование по неорганической химии за курс 8 – 9 класса
Вариант III
1. Однородная смесь
А) мел и вода В) воздух
С) бензин и вода D) молоко Е) железо и сера
2.Признак химической реакции
А) изменение формы В) плавление
С) замерзание D) появление запаха Е) испарение
3.Тип реакции: CaO + 2HCl = CaCl2 + H2O
А) разложения В) соединения
С) обмена D) замещения Е) дегидрирования
4.Кислород нельзя получить разложением
А) KClO3 В) H2O
С) KMnO4 D) HgO Е) CaCO3
5. Кислотный оксид
А) FeO В) Al2O3
С) SO3 D) CaO Е) Na2O
6. Для реакции с 4г оксида меди(II) необходим водород количеством вещества
А) 0,5 моль В) 0,05 моль
С) 0,125 моль D) 0,0125 моль Е) 0,25 моль
7.Формула двухосновной бескислородной кислоты
А) H2SO3 В) HCl
С) H3PO4 D) H2SO4 Е) H2S
8. Относительная молекулярная масса нитрата магния
А) 148 В) 112
С) 90 D) 174 Е) 106
9. Не является свойством воды
А) без запаха В) твёрдая при 200С
С) плохо проводит электрический ток
D) плотность в твёрдом состоянии меньше, чем в жидком Е) кипит при 1000С
10.Сумма коэффициентов в молекулярном уравнении реакции взаимодействия кальция с водой
А) 3 В) 8
С) 4 D) 6 Е) 5
11.Для реакции с 16г сульфата меди(II) необходим гидроксид калия массой
А) 2,8г В) 16,8г
С) 5,6г D) 22,4г Е) 11,2г
12. Формула вещества Х в схеме превращений Вa → ВaO → Вa(OH)2 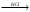 Х
Х
А) Вa(OH)2 В) ВaCl2
С) Вa D) Вa(NO3)2 Е) ВaCO3
13.Ряд чисел 2,8,3 соответствуют распределению электронов по энергетическим уровням атома
А)Al В)N
С)P D)Cl Е)S
14. Число нейтронов в ядре атома меди 64Cu
А) 32 В) 25
С) 27 D) 39 Е) 35
15. Наиболее выражены неметаллические свойства
А) O В) S
С) Se D) Te Е) Po
16.Число протонов в атоме определяется по
А) порядковому номеру элемента В) номеру группы
С) номеру периода D) номеру ряда Е) атомной массе
17. Ионная связь в молекуле
А) НCl В) Cl2
С) CaCl2 D) NH3 Е) P2О5
18. Степень окисления серы в сульфиде калия K2S
А) +1 В) +2
С) -2 D) +4 Е) -4
19. Неэлектролит
А) NaCl В) K2CO3
С) HNO3 D) C6H12O6 Е) Na2CO3
20. Сокращённое ионное уравнение: 2H++CO32-=H2O+CO2 соответствует взаимодействию
А) CaCO3 + 2HCl→ В) Na2CO3 + H2SiO3→ С) CaCO3 + H2SiO3 →
D) Na2CO3 + 2HCl → Е) BaCO3 + 2HCl →
21. Неметаллу соответствует электронная формула
А) 1s22s22p63s1 В) 1s22s22p63s2
С) 1s22s22p63s23p1 D) 1s22s22p63s23p3 Е) 1s22s2
22. Число молекул в 35,5г хлора Cl2
А) 6,02∙1023 В) 6,02∙1022
С) 3,01∙1023 D) 9,03∙1023 Е) 3,01∙1022
23. Массовая доля серы в оксиде серы (IV)
А) 50% В) 25%
С) 40% D) 80% Е) 65%
24. При взаимодействии 32 г меди с 22,4 л кислорода образуется оксид меди (II) массой
А) 40 г В) 80 г
С) 60 г D) 20 г Е) 90г
25. Элемент «Э» в схеме превращений Э → Э2О5 →Н3ЭО4
А) сера В) кальций
С) хлор D) углерод Е) фосфор
26. Сумма коэффициентов в уравнении реакции полного сгорания угля
А) 3 В) 4
С) 5 D) 6 Е) 7
27. Только металлы расположены в ряду
А) N, Na, Li В) Ca, Sr, Ba
С) As, Mg, P D) Cl, Br, I Е) Be, H, B
28. Наименьший радиус атома
А) Na В) K
С) Cs D) Li Е) Fr
29. Cхеме Ca0-2ē → Ca2+ соответствует реакция
А) CaCO3 + 2HCl →CaCl2+ H2O + CO2
В) CaCl2 + 2NaOH →Ca(OH)2 + 2NaCl
С) CaO + CO2 → CaCO3
D) CaH2 + 2H2O → Ca(OH)2 + 2H2
Е) Ca + 2HCl → CaCl2 + H2
30. При сгорании 5,4г алюминия образуется оксид алюминия массой
А) 5,1г В) 7,5г
С) 10,2г D) 15г Е) 6,1г







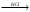 Х
Х

















