ТОТЫҒУ – ТОТЫҚСЫЗДАНУ РЕАКЦИЯЛАРЫ
13.1 Тотығу дәрежесі
Тотығу дәрежесі деп – атомда электрон жұбының терісэлектрлігі жоғары атомға ығысқан кездегі зарядты атайды. Тотығу дәрежесі «n» әріпімен белгіленеді. Молекулаладағы атомның тотығу дәрежесін анықтау үшін мынандай жағдайларға сүйену қажет:
а) Жай зат атомдарының тотығу дәрежелері нольге тең, себебі: бұл жағдайда атомдардың терісэлектрлігі бірдей, электрон жұбының ығысуы болмайды. Мысалы: Cl2 Cl  Cl немесе nCl = 0
Cl немесе nCl = 0
ә) Иондық қосылыстардағы атомдардың тотығу дәрежелері шамасы және таңбасы ионның зарядына тең: Na+Cl-, nCl = -1 (таңбасы санның алдына қойылады).
1) Ковалентті қосылыстардың атомдарының тотығу дәрежесі терісэлектрлігі жоғары атомға ығысқан электрон жұп санымен анықталады. Мысалы, H3N n = 3; n=+1, яғни терісэлектрлігі жоғары атомның тотығу дәрежесі «-» таңбалы санмен, ал оң электрлі атомның тотығу дәрежесі «+» таңбалы санмен белгіленеді.
Н+ → N-3 ← H+
↑
H+
2)Молекула құрамындағы атомдардың тотығу дәрежелерінің алгебралық қосындысы әрқашан нольге тең.
+1 +6 -2
Na2 S O4 2*(+1) + 1*(+6) + 4*(-2) = 0
Фтордың тотығу дәрежесі барлық қосылыстарында «-1»-ге, оттегінікі «-2»-ге тең.
ОҒ2, Ғ-1 ← О+2 → Ғ-1, n0 = +2; H2O2 H+1 → O-1 ÷ O-1 ← H+1; n0 = -1
Сутегінің тотығу дәрежесі гидридтерден басқа қосылыстарында «+1»-ге тең.
СаН2 Н-1 – Са – Н-1 nH = -1.
Тотығу дәрежесі бөлшек сан болуы мүмкін:
Н+1N-1/3; K+1O3-1/3 (калий озониді)
Көптеген жағдайларда тотығу дәрежесі валенттілікке, яғни атомдардың байланыстар санына тең болмайды.


 N20, N2-2H4, NH2OH, азоттың валенттілігі 3-ке тең, ал тотығу дәрежесі әртүрлі: Н+→ N-2 – N-2 ← H+ H+ → N→ O-2 ← H+
N20, N2-2H4, NH2OH, азоттың валенттілігі 3-ке тең, ал тотығу дәрежесі әртүрлі: Н+→ N-2 – N-2 ← H+ H+ → N→ O-2 ← H+
N0≡N0 H+ H+ H+
Яғни, егер молекуланың құрылымы белгілі болса, «n»-анықтау оңай. Ал егер молекуланың құрылымы белгісіз болса, тотығу дәрежесін анықтау үшін 4 және 5 ережеге сүйену керек. Мысалы, Ca(NO3)2 молекуласындағы азоттың тотығу дәрежесін анықтау үшін:
Молекулада – 1 атом кальций, nCa = +2
2 атом азот, nN = x;
3 атом оттегі, nO = -2.
Молекуланы құрайтын атомдардың тотығу дәрежелерінің қосындысы нөлге тең болатындықтан:
1*(+2) + 2*(х) + 6*(-2) = 0
+2 + 2х – 12 = 0
2х = +10
х = +5 n(N) = +5
Мына заттардың тотығу дәрежелерін анықтаңдар:
nC CH4, CH3Cl, CH2Cl2, CHCl3, CCl4
nCr H2CrO4, K2Cr2O7, H2CrO6, CrO3
nS K2S, SO2, Fe2(SO4)3
Күкірт пен көміртегі қосылыстарының графикалық формулаларын жазып, электрон жұптарының ығысуын көрсет.
Тотығу дәрежесі туралы түсінкі тотығу – тотықсыздану реакцияларын оқуда маңызы зор. Бұл реакцияларда, электрондардың бір атомнан екінші атомға толық ауысуының немесе тартылуының нәтижесінде тотығу дәрежелері өзгереді.
Әрекеттесетін заттардың құрамындағы атомдардың тотығу дәрежелері өзгере жүретін реакциялар тотығу – тотықсыздану реакциялары деп аталады.
С0 + О20 → СО2
Тотығу дәрежелерінің өзгеруі электрондардың ауысуына байланысты. Тотығу – тотықсыздану реакцияларының электрондық теориясының негізгі жағдайлары:
Тотығу – молекулалардың, атомдардың немесе иондардың электрон беру процесі.
Zn - 2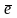 → Zn2+
→ Zn2+
H2 - 2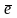 → 2H+
→ 2H+
2Cl- - 2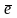 → Cl2
→ Cl2
2)Тотығу – тотықсыздану – атомдардың, молекулалардың немесе иондардың электрон қосып алу процесі.
S + 2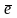 → S2-
→ S2-
Cl2 + 2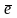 → 2Cl-
→ 2Cl-
Электрон беретін атомдар, молекулалар немесе иондар тотықсыздандырғыштар деп аталады. Реакция кезінде олар тотығады.
Электрон қосып алатын атомдар, молекулалар немесе иондар тотықтырғыштар деп аталады. Реакция кезінде олар тотықсызданады.
Тотығу процесі - әрқашан тотықсыздануымен қатар жүреді және керісінше. Сондықтан тотығу-тотықсыздану реакциялары екі қарама – қарсы процесс тотығу мен тотықсызданудың бірігуі болып табылады.
13.2 Тотығу – тотықсыздану реакцияларын электрондық баланс әдісімен және ионды – электронды әдісімен теңестіру.
Электрондық баланс әдісі – бастапқы және соңғы зат атомдарының тотығу дәрежелерін салыстыруға негізделген.
Оның негізінде тотықсызданатын берген электрон саны тотықтырғыштың қосып алған электрон санына тең болу ережесі жатыр.
Бұл әдісті күкіртті сутек және калий перманганатының (қышқыл ортада) әрекеттесуінің реакция теңдеуін құрастыру арқылы түсіндірейік:
1)Алдымен реакция схемасын, яғни бастапқы заттарды және реакция өнімдерін жазамыз:
H2S + KMnO4 + H2SO4 → S + MnSO4 + K2SO4 + H2O
2) Атомдардың реакцияға дейінгі және реакциядан кейінгі тотығу дәрежелерінің өзгеруін анықтау:
H2S-2 + KMn+7O4 + H2SO4 → S0 + Mn+2SO4 + K2SO4 + H2O
Бұдан күкірт пен марганецтің тотығу дәрежесінің өзгергенін көреміз.
3) Сонан соң электрондық теңдеулерін құрастырамыз, яғни электрон беру және қосып алу схемаларын жазамыз:
S-2 -2 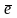 → S0 5
→ S0 5
 Mn+7 + 5
Mn+7 + 5 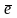 → Mn+2 2
→ Mn+2 2
4) Тотықтырғыш пен тотықсыздандырғыш коэффициенттерін табамыз, оларды реакция схемасына жазамыз.
5) Басқа әрекеттесуші заттардың алдына коэффициенттерін қоямыз. Реакцияның соңғы теңдеуі мынадай түрде жазылады.
5H2S + 2KMnO4 + 3H2SO4 → 5S + 2MnSO4 + K2SO4 + 8H2O
6) Теңдеудің оң және сол жағындағы элемент атомдарын санау арқылы, коюффициенттердің қойылуының дұрыстығын тексереміз.
Ионды – электронды әдіс. Ионды – электронды әдіспен тотығу – тотықсыздану реакцияларын теңестіру үшін төмендегідей ережелер қолданылады:
1) Тотығу – тотықсыздану реакциясына қатысатын қосылыстардың тотығу дәрежесі емес, ион заряды анықталады:
KMnO4 + KJ + H2SO4 → MnSO4 + J2 + K2SO4 + H2O
K+ + MnO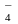 + K+ + J-+2H+ + SO
+ K+ + J-+2H+ + SO → Mn2+ + SO
→ Mn2+ + SO + J2 + 2K+ + SO
+ J2 + 2K+ + SO + H2O
+ H2O
2) Тотықтырғыш пен тотықсыздандырғышты анықтап, тотығу – тотықсыздану үрдісінде шынайы қатысатын иондарды көрсете отырып, химиялық реакцияның иондық сызбанұсқасын құраймыз:
MnO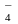 + J- + H+ → Mn2+ + J0 + H2O
+ J- + H+ → Mn2+ + J0 + H2O
MnO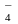 ионы Mn2+-ке дейін тотықсызданып, J- - ионы J0 – ге дейін тотығады. Реакция кезінде сутегі ионының қатысуы реакцияның қышқылдық ортада өтетіндігін көрсетеді. Бұл әрі қарай тұжырым жасауға көмектеседі.
ионы Mn2+-ке дейін тотықсызданып, J- - ионы J0 – ге дейін тотығады. Реакция кезінде сутегі ионының қатысуы реакцияның қышқылдық ортада өтетіндігін көрсетеді. Бұл әрі қарай тұжырым жасауға көмектеседі.
3) Әрбір жартылай реакция теңдеуі үшін электронды - иондық теңдеу құрастырылады. Егер бастапқы алынған затта оттегі саны көп болса, онда сол жақ бөлігіне оттегіні байланыстыруға қажетті сутегі ионы қосылады. Ал теңдеудің оң бөлігіне судың сәйкес келетін молекула саны жазылады.
MnO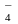 + 8H+ + 5
+ 8H+ + 5 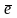 → Mn2+ + 4H2O
→ Mn2+ + 4H2O
Әрбір жарты реакция теңдігіндегі электрон саны ион зарядтарының қосындысына тең болу керек.
 2J- - 2
2J- - 2 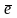 → J2 екінші жартылай реакция
→ J2 екінші жартылай реакция
2J- - 2 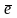 → J2 5 тотығу
→ J2 5 тотығу
MnO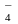 + 8H+ + 5
+ 8H+ + 5 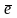 → Mn2+ + 4H2O 2 тотықсыздану
→ Mn2+ + 4H2O 2 тотықсыздану
2MnO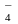 + 10J- + 16H+ → 2Mn2+ + 5J2 + 8H2O
+ 10J- + 16H+ → 2Mn2+ + 5J2 + 8H2O
Әрбір жартылай реакция теңдеуінің көбейткішке көбейтіп, тотығу – тотықсыздану үрдісіндегі электрон санын теңестіреміз. Осыдан кейін әрбір жартылай реакция теңдеуін қосып, толық реакция теңдеуін аламыз.
Ионды – электронды реакцияның артықшылығы:
«Тотығу дәрежесі» формальды түсінігін қолданбаймыз;
Тотығу – тотықсыздану реакциясындағы орта әсерін анықтауға мүмкіндік береді.
13.3 Тотықтырғыш пен тотықсыздандырғыштардың эквиваленті
Тотықтырғыш пен тотықсыздандырғыш әрқашан өзара өздерінің тотығу-тотықсыздану эквиваленттігіне қатысты әрекеттеседі.
Тотықтырғыштың эквиваленті деп – тотықтырғыштың осы берілген реакциядағы бір электрон қосып алатын мөлшері. Тотықтырғыштың эквивалентін есептеу үшін оның молекулалық массасын бір молекуланың қосып алған электрон санына бөледі.
Тотықсыздандырғыштың эквиваленті деп – осы берілген реакциядағы бір электронды беретін тотықсыздандырғыштың мөлшері. Тотықсыздандырғыштың эквивалентін табу үшін молекулалық массасын тотықсыздандырғыштың берген электрондар санына бөледі.
Э = 
мұндағы, Э-тотықсыздандырғыштың не тотықтырғыштың эквиваленті, М – молекулалық масса, n - молекуланың, атомның немесе ионның берген не қосып алған электрон саны. Мыс пен концентрлі азот қышқылының әрекеттесу тәжірибесін жасау. Реакция теңдеуін жазу. Тотықтырғыш пен тотықсыздандырғыштың эквивалентін есептеу.
13.4 Тотығу – тотықсыздану реакцияларының типтері
Тотығу – тотықсыздану реакцияларын үш топқа бөледі:
Молекулааралық тотығу – тотықсыздану реакциялары;
Диспропорциялау немесе өздігінен тотығу – тотықсыздану реакциялары;
Молекулаішілік тотығу – тотықсыздану реакциялары.
Электрон алмасу әртүрлі молекулалар арасында жүретін реакциялар – молекулааралық деп аталады.
K2Cr2O7 + 7H2SO4 + 6FeSO4 → Cr2(SO4)3 + 3Fe2(SO4)3 + K2SO4+7H2O
Cr+6 – тотықтырғыш (K2Cr2O7-де)
Ғе+2 – тотықсыздандырғыш (FeSO4-те).
Бір ғана заттың молекулалары және иондары бір-бірімен тотықтырғыш және тотықсыздандырғыш сияқты реакцияласуын диспропорциялау реакциялары деп атайды.
HCl+5O3 + 3HClO3 = HCl +3HClO3
Cl+5 – тотықтырғыш (HClO3)
Cl+5 – тотықсыздандырғыш (басқа HClO3 молекулаларда)
Сол бір заттың құрамындағы тотықтырғыш және тотықсыздандырғыш ролін әр түрлі элемент атомдары атқаратын реакция молекулаішілік тотығу-тотықсыздану реакциясы деп аталады.
2AgCl = 2Ag + Cl2
 Ag+ - тотықтырғыш AgCl-ң бір молекуласында
Ag+ - тотықтырғыш AgCl-ң бір молекуласында
 Cl- - тотықсыздандырғыш
Cl- - тотықсыздандырғыш
Келесі теңдеулердегі реакциялар қай типке жататынын анықтау:
2N+4O2 + H2O = HN+3O2 + HNO3
2KmnO4 = K2MnO4 + MnO2 + O2
Zn + 2H2SO4 = ZnSO4 + SO2 + H2O
13.5 Маңызды тотықтырғыштар мен тотықсыздандырғыштар
Барлық жай заттарды тотығу – тотықсыздану қасиетіне байланысты 3 топқа бөлуге болады:
Тек тотықтырғыштық қасиет көрсететін заттар. Бұл қасиет тек фторға тән.
Тек тотықсыздандырғыштық қасиет көрсететін заттар. Бұл қасиетке металдар, 1, 2, 3 топтың (бордан басқа) қосымша және негізгі топша элементтерінің атомдарынан жасалған барлық жай заттар жатады.
Тотықтырғыш та тотықсыздандырғышта қасиет көрсететін жай заттар (буған 4-7 топтың негізгі топша элементтерінің атомынан құралған жай заттар жатады).
Күрделі заттардың тотығу-тотықсыздану қасиеті берілген элемент атомының дәрежесіне байланысты. Егер элемент максимальді тотығу дәрежесіне ие болса және оны ары қарай көтере алмаса (яғни электрон бермесе), онда бұл зат тек тотықтырғыш болады. Егер элемент атомының тотығу дәрежесі минимальді болса, онда зат тотықсыздандырғыш қасиет көрсетеді. Мысалы, азот 5 топтың негізгі топшасында орналасқан, оның максимальді валенттілігі 5, тотықсыздану дәрежесі +5, минимальді тотығу дәрежесі +3.
HNO3 – тек тотықтырғыш;
NO2, HNO2, NO, N2O, N2, NH2OH, N2H4 – бұл жағдайда азот атомы аралық тотығу дәрежесін көрсетіп, тотықтырғыш та тотықсыздандырғыш та қасиет көрсетеді.
NH3 – тек тотықсыздандырғыш қасиет көрсетеді.
Маңызды тотықтырғыштар:
KMnO4 қою көгілдір ерітінді – қышқыл ортада Mn+2 (түссіз)
KMnO4 қою көгілдір ерітінді – бейтарап ортада MnO2 (сұр түсті)
KMnO4 қою көгілдір ерітінді – сілті ортада MnO4 (жасыл түсті ерітінді)
Маңызды тотықсыздандырғыштар: металдар, сутегі, хлорсутек, бромсутек. Тотығу-тотықсыздану қасиетін көрсететін заттардан күкіртті қышқыл және оның тұздарын, азот қышқылын және оның тұздарын, сутек пероксидін т.б. атауға болады.
-2 0 +4 +6
H2S ← S ← H2SO3 → H2SO4
-3 0 + +2 +3 +4 +5
2) H3N ← N2 ← N2O ←NO ← HNO2 → NO2 → HNO3
H2O2 – тотықтырғыш;
H2O2 – қышқыл ортада H2O2 +2Н+ +2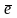 → 2 H2O2
→ 2 H2O2
H2O2 – бейтарап немесе сілтілік ортада H2O2 +2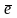 → 2ОН-
→ 2ОН-
H2O2 – тотықсыздандырғыш;
H2O2 – 2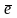 → О2 + 2Н+
→ О2 + 2Н+






 Cl немесе nCl = 0
Cl немесе nCl = 0

 N20, N2-2H4, NH2OH, азоттың валенттілігі 3-ке тең, ал тотығу дәрежесі әртүрлі: Н+→ N-2 – N-2 ← H+ H+ → N→ O-2 ← H+
N20, N2-2H4, NH2OH, азоттың валенттілігі 3-ке тең, ал тотығу дәрежесі әртүрлі: Н+→ N-2 – N-2 ← H+ H+ → N→ O-2 ← H+ → Zn2+
→ Zn2+ Mn+7 + 5
Mn+7 + 5  + K+ + J-+2H+ + SO
+ K+ + J-+2H+ + SO → Mn2+ + SO
→ Mn2+ + SO 2J- - 2
2J- - 2 









