Урок по теме : Повторение и обобщение знаний по теме Металлы
Эпиграф нашего урока: «Мощь и сила науки-
во множестве фактов,
цель – в обобщении этого множества»
Д.И.Менделеев.
Цели: Повторить и обобщить знания по пройденной теме, закрепить умения и навыки составлять формулы, осуществлять превращения, решать задачи, развивать умения логически мыслить ,делать выводы. Воспитывать самостоятельность, ответственность при выполнении работы.
Оборудование: листочки для с/р, реактивы: хлорид железа(3), сульфат алюминия, гидроксид натрия, горючее, медная проволочка, хлорид бария, соляная кислота, пробирки.
Ход урока.
Мы заканчиваем изучение курса неорганической химии и уже на ближайших уроках займемся рассмотрением нового раздела химической науки – органической химии. Но прежде нам необходимо вспомнить основные вопросы, изученные в этом учебном году. Еще Йенс Якоб Берцелиус условно разделил все известные тогда химические элементы на металлы и неметаллы. Это деление весьма условно. Но именно эти химические элементы образуют простые вещества неметаллы и металлы. Семь металлов создал век По числу семи планет: Медь, железо, серебро… Дал нам Космос на добро. Злато, олово, свинец…Сын мой сера – их отец. И еще ты должен знать,Всем им ртуть - родная мать. Именно металлам мы посвятим сегодняшний урок. Обратим внимание на эпиграф, записанный на доске. Прочитайте его внимательно и в конце урока мы прокомментируем эти слов. Начинаем повторение:
1.Викторина 1.К амфотерным оксидам относится
 оксид цинка
оксид цинка
 оксид магния
оксид магния
 оксид меди (II)
оксид меди (II)
 оксид азота (IV)
оксид азота (IV)
2.К щелочам относится гидроксид
 углерода (IV)
углерода (IV)
 железа (II)
железа (II)
 натрия
натрия
 алюминия
алюминия
3.Три электрона находятся во внешнем электронном слое атома
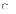 углерода
углерода
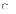 мышьяка
мышьяка
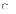 алюминия
алюминия
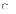 лития
лития
4.Cколько электронов находится на внешнем уровне элемента с порядковым номером 13?—3—5-- 13
Вопросы для команд"А", "В","С". Первый раунд 1.Самый легкий из всех металлов? (Литий) 2.Название какого радиоактивного металла происходит от названия одной из планет солнечной системы?(Нептуний) 3.Бытовое название продукта разрушения железа под воздействием внешней среды?(Ржавчина) 4.Способ получения металлов с помощью электрического тока?(Электролиз) 5.Первый металл, который был обработан человеком?(Медь) 6.Какое важнейшее механическое свойство металлов лежит в основе кузнечного дела?(Пластичность) 7.Амальгамы - это растворы металлов в ...?(Ртути) 8.Металл, используемый в медицине при рентгенографии как защиту от излучения.(Свинец) 9.Какой металл содержится в природном минерале магнетите?(Железо) 10.Атом какого металла содержит в два раза больше протонов, чем магний?(Хром) 11.Самый тугоплавкий из всех металлов?(Вольфрам) 12.Какие два элемента - металла названы в честь частей света?(Европий, Амереций) 13.Именем какого небесного тела алхимики называли серебро?(Луны) 14.Самый распространенный металл на Земле?(Алюминий) 15.Какое уникальное свойство железа находит применение в микрофонах(Ферромагнетизм) 16.Какой металл используется в изготовлении сигнальных осветительных ракет?(Магний) 17.Из какого металла размером со спичечную головку можно вытянуть проволоку 3км длиной и расплющить лист площадью 50 кв.м?(Золото) 18.Американские ученые - токсикологи считают, что одной из причин падения Рима является отравление его жителей металлом, используемого для изготовления труб водопровода, а также дорогой посуды и косметических средств. Какой это металл?(Свинец) Экспериментальная пауза Второй раунд 1.Сколько процентов золота содержится в кольце 585 пробы?(58,5%) 2.Назовите главный металл электротехники.(Медь) 3.О каком металле говорят: Металл - и плуг в поле, и гвоздь в доме?(Железо) 4.Самый тяжелый из известных металлов(Осмий) 5.Металл, дающий при сгорании яркий белый свет, что ранее находило применение в качестве вспышки при фотографировании?(Магний) 6.Металл, способный расплавляться теплотой ладони и называемый небесно - голубым или лазоревым?(Цезий, 28,5С) 7.Щелочной металл по имени которого называют группу минеральных удобрений?(Калий) 8.Какой металл алхимики обозначали в виде копья и щита - характерных атрибутов войны и Марса?(Железо) 9.Какой металл является основой сплавов, таких как бронза, мельхиор, латунь?(Медь) 10.На некоторых древних языках этот металл называли "небесным камнем"?(Железо) 11.Какой ядовитый металл обезвреживают демеркуризацией?(Ртуть) 12.Название страны Южной Америки, Аргентины произошло от названия металла ...(Серебро) 13.Какой из благородных, драгоценных металлов чаще всего используют в качестве катализатора при химических процессах?(Платина) 14.Металл, являющийся основой современной цивилизации?(Железо) 15.Какие металлы из - за легкости и высокой химической активности хранят под слоем керосина?(Щелочные, щелочноземельные) 16.Металл, являющийся лучшим проводником электрического тока и тепла.(Серебро) 17.Есть загадочный металл, в воду бросишь - побежал. По поверхности кружился, пошипел и вдруг пропал. О каком металле это четверостишье?(Натрий) 18.Присутствие ионов какого металла обнаруживают красной и желтой кровяными солями?(Ионы железа (ii) и (iii) Экспериментальная пауза Третий раунд 1.Какой металл называют крылатым?(Алюминий) 2.Что объединяет такие металлы как франций, радий, полоний?(Радиоактивны) 3.Ионы какого металла уничтожают бактерии и даже в незначительной концентрации стерилизуют питьевую воду?(Серебра) 4.Металл,имеющий высокую биологическую совместимость с животными тканями и применяемый в хирургии?(Тантал) 5.Как выделить железные опилки из смеси, содержащей кроме железа, песок, поваренную соль и серу?(Магнитом) 6.Сегодня данный металл довольно дешевый и широко распространен, а в 1854г. его стоимость составляла 1200 руб. за 1 кг, что в 270 раз дороже серебра. На Всемирной выставке в 1855г. его демонстрировали как материал для ювелирных украшений.(Алюминий) 7.Название частиц, расположенных в узлах кристаллических решеток металлов.(Атом - катионы) 8.Какой металл по мнению алхимиков рождался в недрах Земли под влиянием лучей планеты Венера?(Медь) 9.Название металла и его свойства, используемого в огнестрельном оружии.(Свинец, высокая плотность) 10.Ядовитый металл, содержащийся в лампах дневного света.(Ртуть) 11.Соединением какого металла повышают октановое число бензина?(Свинца - тетраэтилсвинец) 14.Какой металл может "болеть"чумой?(Олово) 15.Хлорид какого металла применяют в медицине для повышения свертываемости крови?(Кальция) 16.Металл, названный в честь России.(Рутений) 17.Какой металл в переводе с латинского называют "серебряной водой"?(Ртуть) 18.Этот металл отличает исключительная химическая стойкость. На него не действуют ни кислоты, ни щелочи. Его может растворить лишь грозная "царская водка."Какой это металл?(Золото)
2.Допиши:
| 1вариант | 2вариант |
| K + O2 = Ba + H2O = K + Cl2 = Mg + S = CaO + HCl= Al + FeCl2= | Ba + O2 = K + H2O = Ca + Cl2 = K + S = MgO + HCl = Ca+ ZnCl2 = |
3.Выполнение заданий по теме «Окислительно – восстановительные реакции».
Одним из химических свойств металлов является их взаимодействие с кислотами. При взаимодействии кислот с металлами выделяется водород, но по другому себя с кислотами ведут азотная и серная кислота. Уравняйте, используя метод электронного баланса следующие химические реакции:
1)Zn+H2SO4 = ZnSO4+SO2↑+H2O 2) Zn+H2SO4 = ZnSO4+ H2S↑+ H2O 3) HNO3 +Ca= Ca(NO3)2+ N2O↑+ H2O 4) HNO3 +Cu= Cu(NO3)2+ NO↑+ H2O
4. Решение задач по теме «Металлы».
Задача №1 Вычислите массу сульфата цинка, который можно получить при взаимодействии избытка цинка с 500мл. 20% раствора серной кислоты с плотностью 1,14 г/мл. Задача №2 К раствору, содержащему 27 г. хлорида меди (II), добавили 14 г. железных опилок. Вычислите массу меди, которая выделилась в результате этой реакции.
5.Назовите :самый, самый металл. (легкий – литий ,тяжелый – осмий, твердый – хром, тугоплавкий – вольфрам, легкоплавкие – цезий и галлий ,жидкий – ртуть) 6.Графический диктант:1 вариант литий 2 вариант кальций 3 вариант бериллий 4 вариант калий Укажите свой вариант.
Вопросы графического диктанта
Является самым легким металлом.
Содержит 1 электрон на внешнем энергетическом уровне.
Его получают электрометаллургическим методом.
При горении в кислороде образует пероксид.
Во всех соединениях имеет степень окисления +2.
На воздухе его поверхность покрывается защитной пленкой.
Его открыл ученый Дэви.
Наличием солей этого металла обусловлена жесткость воды.
В переводе с греческого языка его название означает камень.
Взаимодействует с неметаллами. Ключ ответов представлен на доске, проверьте правильность выполнения заданий и оцените вашего товарища, выставив ему объективную оценку. Критерии выставления оценок записаны на доске.
7.Осуществить превращения:
1.Сu → CuO → CuSO4 → Cu(OH)2 → CuO → Cu 2. Mg → MgCl2 → Mg(OH)2 → MgSO4 → MgCO3 → MgO
8. конкурс - «Очумелые ручки».
Задание: , проделайте реакции, подтверждающие качественный состав:
1 команды - хлорида железа (III); 2 команды – сульфата алюминия.
Запишите соответствующие уравнения реакций в молекулярном виде.
«Черный ящик»
Спрятан в ящике предмет –
Без него не съесть обед.
Вещь незаменимая,
Вещь необходимая.
Если мы садимся кушать,
Тот предмет нам очень нужен.
Из чего же сей предмет?
Серебристо-белый цвет
Вам позволит дать ответ.
(Алюминиевая ложка, вилка)
Д/З Подготовиться к контрольной работе.
















