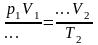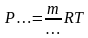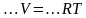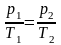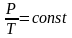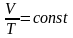Областное бюджетное образовательное учреждение
среднего профессионального образования
«Курский монтажный техникум»
Преподаватель: Шелкова М.С.
Газовые законы. Закон Бойля-Мариотта.
(Методическая разработка открытого занятия по физике)
Курск 2014
Тема: Газовые законы. Закон Бойля-Мариотта.
Тип занятия: комбинированный.
Цели:
- образовательная: проверка усвоения теоретических знаний о
газовых законах, совершенствование умений
использования закона Бойля-Мариотта;
- воспитательная: воспитание чувства ответственности за свою
деятельность, совершенствование умения работать в
группе, развитие мотивации к изучению предмета;
- развивающая: развитие творческих способностей: память, внимание,
воображение; развитие логического мышления и
способности к систематизации знаний, анализу изученного
материала.
Задачи:
- повторить и обобщить ранее изученный материал по обозначенной теме;
- продолжить формировать умения использовать полученные знания при решении практико-ориентированных задач;
- совершенствовать знания обучающихся и способствовать самостоятельному использованию данных знаний на практике;
- активизировать учебную деятельность исследовательского характера посредством проведения эксперимента;
- совершенствовать навыки использования различных измерительных инструментов.
Оборудование: интерактивная доска, автоматизированное рабочее место
преподавателя, ручки, стеклянная банка 2л, воздушный
шарик, две пластиковые банки с крышкой, сосуд с холодной
водой, горячая вода, пустой сосуд, пластиковая бутылка 1,5 л
заполненная водой, медицинская пипетка, заполненная
подкрашенной водой, приборы лабораторной работы.
Наглядные средства: презентация, карточки для проведения рефлексии
эмоционального состояния.
Методический материал: карточки с заданиями, методические указания к
выполнению лабораторной работы с бланками
отчета.
План
Организационный момент. (1-2 мин.)
Рефлексия эмоционального состояния (1-2 мин.)
Постановка проблемной ситуации. (5-7мин.)
Активизация знаний. (7-10 мин.)
Рефлексия эмоционального состояния (1-2 мин.)
Решение задач. (5-7 мин.)
Объяснение задания лабораторной работы. (3-5 мин.)
Физическая минутка. (2-3 мин.)
Инструктаж по технике безопасности. (1-2 мин.)
Проведения опыта и оформление отчета. (15-20 мин.)
Формулировка вывода. (3-5 мин.)
Формулировка темы лабораторной работы (3-5 мин.)
Рефлексия изученного материала (3-5 мин.)
Подведение итогов занятия. (1-2 мин.)
Рефлексия эмоционального состояния (1-2 мин.)
Окончание занятия. (1-2 мин.)
Ход занятия
Организационный момент.
П: Здравствуйте уважаемые студенты, садитесь пожалуйста! По традиции, сначала проверим отсутствующих.
Сегодня на занятии мы с вами вспомним выдающихся ученых, которые внесли вклад в развитие молекулярной физики. Вы узнаете почему из крана иногда течет «молочная вода», в чем польза зевоты и многое другое. Наше занятие будет посвящено газовым законам.
Рефлексия эмоционального состояния.
П: Но в начале нашего занятия мне бы очень хотелось узнать ваше настроение. Для этого прошу поднять квадрат того цвета, который сейчас соответствует вашему эмоциональному состоянию. Красный квадрат - «хуже не бывает», желтый – «так себе», зеленый - «отличное» (комментарии по результату).
Постановка проблемной ситуации.
П: А сейчас предлагаю вам посмотреть видео эксперимент (демонстрация видео опыта). Как было показано в данном опыте, вывод должен соответствует закону Бойля-Мариотта, открытому двумя величайшими учеными в разное время – англичанином Робертом Бойлем в 1662 г. и французом Эдмом Мариоттом в 1667г. А соответствует он или нет мы с вами и проверим при выполнении лабораторной работы.
Активизация знаний.
П: Для этого прежде всего необходимо вспомнить некоторые понятия и величины по теме газовые законы.
Задание 1: Заполните пропущенные слова в определениях.
Идеальный газ – ………… реального газа, в которой пренебрегают ………. молекул и взаимодействие между молекулами………………
Состояние идеального газа характеризуется ….. параметрами состояния: давление,…………. и температура.
Изопроцессы – это процессы протекающие при …… значении одного из параметров.
Задание 2: Допишите формулы:
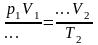
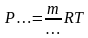
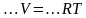

Задание 3: Построим дом знаний (Заполняют блоки по законам. После каждого блока показывают опыт).
П: Сегодня газовые законы легко можно вывести из уравнения состояния идеального газа. Но первоначально они были получены экспериментальным путем, часто даже сами ученые не придавали значения полученным результатам. И только лишь спустя некоторое время, по мере формирования науки о тепловых явлениях, приходило понимание фундаментальности полученных взаимосвязей.

Уравнение Клапейрона (m = const): 
| Уравнение для двух состояний | 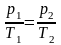
| V1T1=V2T2
| P1V1=P2V2
|
| Название изопроцесса | изохорный | изобарный | изотермический |
| Газовый закон (постоянный параметр) | V=const | P=const | T=const
|
| Газовый закон (зависимость) | 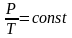
P~T
| 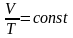
V~T |
PV=const P~1/V |
| Газовый закон (название, год открытия) | Закон Шарля 1787г. | Закон Гей-Люссака 1802г. | Закон Бойля-Мариотта 1662г., 1667г.
|
| Эксперимент | Р увеличивается при нагревании газа в баллоне (V= const) | При нагревании газа в цилиндре с подвижным поршнем происходит его изобарное расширение, если Рвнеш. =Ратмосф=const. | Медленное сжатие или расширение газа, чтобы Т не успела измениться. |
а) Чтобы проиллюстрировать изохорный процесс посмотрим опыт “Разрушение банки”.
Оборудование: пластмассовая или металлическая банка с закручивающейся крышкой, очень горячая вода, сосуд с холодной водой.
Опыт: налить горячую воду в банку подержать там 2 мин. и вылить, быстро закрыв отверстие. Затем сразу облить ее холодной водой. Банку сплющит.
Объяснение: Во время нагревания вода расширяется, превращаясь в газ – пар. Когда мы закрыли банку крышкой, воздух внутри остался под таким же давлением, как окружающая атмосфера. Охлаждая ёмкость извне, мы заставили пар превращаться обратно в воду. Его давление понизилось, позволяя большему давлению воздуха внешней атмосферы раздавить банку.
б) Чтобы проиллюстрировать изобарный процесс посмотрим опыт “Яйцо в бутылке”.
Оборудование: стеклянная бутылка, вареное яйцо, горячая вода, пустой сосуд.
Опыт: в пустую стеклянную бутылку наливаем горячей воды и держим там 1-2 мин, затем выливаем ее в пустой сосуд. Бутылку накрываем вареным яйцом и наблюдаем, как яйцо втягивается в банку.
Объяснение: при нагревании воздух в банке расширился, и его часть вышла из банки. При охлаждении воздух в банке сжимается, и яйцо втягивается в бутылку под действием атмосферного давления, которое на протяжении всего опыта не менялось.
в) Чтобы проиллюстрировать изотермический процесс посмотрим опыт “Картезианский водолаз”
Оборудование: пластмассовая бутылка 1,5 л, заполненная водой с крышкой; медицинская пипетка, заполненная подкрашенной водой.
Опыт: Бутылка наполненная водой внутри которой плавает пипетка. Закроем плотно колбу крышкой и возьмем колбу в руки – пипетка погружается, уберем руки пипетка всплывает объясните действие пипетки.
Объяснение: когда ведущий берет мягкую бутылку в руки, он ее сдавливает. Это приводит к увеличению давления внутри бутылки и уменьшения объема пузырька воздуха в пипетке, т.е. по закону Бойля-Мариотта увеличение давления на газ (воздух в пипетке) приводит к уменьшению объема этого воздуха (сжатию). При этом уменьшается сила Архимеда и пипетка тонет. Меняя нажим на бутылку, ведущий имеет возможность изменять эту силу и управлять глубиной погружения пипетки. Для этого принципиально важно, чтобы бутылка была герметично закрыта.
Рефлексия эмоционального состояния.
П: Итак, вы просмотрели опыты, демонстрирующие газовые законы. Какое впечатление они произвели на вас. Давайте снова обратимся к вашему эмоциональному состоянию, в каком настроении вы находитесь сейчас? Красный квадрат - «хуже не бывает», желтый – «так себе», зеленый - «отличное» (комментарии по результату).
Решение задач.
П: Я предлагаю вам попробовать себя в роли преподавателя. Пред вами «черный ящик», в котором находятся интересные задания. Вы достаете по одной карточке с вопросом и зачитываете его, а затем спрашиваете любого из ваших одногруппников. Вопросы непосредственно связаны с нашей темой.
Почему при надувании щек увеличивается давление и объем, ведь это противоречит закону Бойля-Мариотта? (В данной задаче закон Бойля-Мариотта не применим, т.к. m ≠ const)
Почему при выливании воды из медицинской грелки не слышно такого «булькания», как при выливании воды из стеклянной бутылки? ( По мере вытекания воды из стеклянной бутылки объём, находящегося над водой воздуха возрастает, согласно закону Бойля-Мариотта, давление уменьшается. Когда разность давлений снаружи и внутри становится достаточно большой, некоторая «порция ) воздуха, т.е. воздушный пузырёк, прорывается внутрь бутылки, создавая характерное «булькание»,. Давление внутри бутылки при этом несколько возрастает. Через некоторое время процесс повторяется. Если же стенки сосуда, из которого вытекает вода, не являются жёсткими, то по мере вытекания воды атмосферное давление сплющивает этот сосуд. Давление внутри сосуда остаётся практически равным атмосферному и «булькание» не возникает.)
Какая польза в зевании? (Зевота (глубокий затяжной вдох и короткий выдох при широко открытом рте) – это рефлекторный акт, являющийся признаком усталости или нехватки кислорода. Однако наряду с проявлением дискомфортного состояния зевота выполняет и защитную функцию для организма. Во время зевания дыхательные пути расширяются, лицевые и челюстные мышцы расслабляются, после чего наступает короткая пауза, во время которой весь организм отдыхает. Следовательно, зевота помогает уставшему организму дольше находиться в состоянии бодрствования.)
Объясните для чего, перед использованием медицинской банки внутрь ее вносят горящий, смоченный спиртом, ватный тампон? (В результате нагревания давление внутри банки увеличивается , а в приложенной к телу остывающей медицинской банке давлении воздуха становится меньше атмосферного и поэтому нагретая медицинская банка «присасывается» к телу. Согласно закону Шарля.)
Иногда из водопроводного крана вода вытекает белая, как молоко. Чем это объясняется? (Воздух растворяется в воде тем лучше, чем больше давление и ниже температура. Когда вода вытекает из крана наружу, давление понижается, а температура повышается, часть воздуха выделяется в виде мелких пузырьков – вода принимает молочно-белый цвет.)
Как изменяется сила, выталкивающая из воды воздушный пузырек, когда он поднимается со дна водоема на поверхность? (Выталкивающая сила пропорциональна объему пузырька, когда пузырек всплывает, выталкивающая сила увеличивается, т.к. объем пузырька возрастает. )
Почему от горящих поленьев с треском отскакивают искры? (Воздух, содержащийся в дереве с возрастанием температуры расширяется, соответственно разрывает волокна дерева и они отскакивают в разные стороны.)
Иногда, из бутылки, наполненной газированной водой, вылетает пробка, если бутылка поставлена в теплое место. Почему? (С увеличением температуры растворимость газов уменьшается, что приводит к увеличению объема, а следовательно к повышенному давлению внутри закрытой бутылки и пробка вылетает.)
Почему баллоны со сжатым газом взрывоопасны, а труба воды под большим давлением взрывобезопасна?(При взрыве трубы с водой давление практически мгновенно падает и не может принести больших разрушений, а при взрыве баллона с газом резко увеличивается объем из-за понижения давления, а следовательно осколки приобретают большие скорости и наносят существенные повреждения.)
Почему в зданиях выше десятого этажа не используют газовое оборудование? (По магистралям газопровода газ поступает с низким давлением, поэтому в целях безопасности выше десятого этажа газовое оборудование не устанавливают.)
П: Любые состояния газа можно описать уравнением состояния: Клапейрона, либо Менделеева-Клапейрона. Эти уравнения содержат в себе, как частные случаи, газовые законы. Газовые законы имеют множество применений в медицине, быту, технике. Внимание на экран. Приведем еще несколько примеров.
1. Пятницкий предложил домашние «туфли пылесос». Каждая туфля имеет между стелькой и подошвой меховую прокладку и пружину. Когда нога с туфлей не опирается на пол, между подошвой и стелькой образуется разрежение, и через отверстия подошвы в пространство устремляется воздух с пылью. В момент опоры на туфли пружины сжимаются, а набранный воздух и пыль перемещаются к каблуку-фильтру.
2. Изучение способности бобров плавать под водой помогает хирургам совершенствовать приёмы проведения операций на открытом сердце. Как только ноздри бобра оказываются в воде, усиливается приток крови к жизненно важным органам, которые наиболее страдают от кислородного истощения. Одновременно уменьшается частота биений сердца, чтобы сократить потребность в кислороде. Этот механизм выполняют нервные окончания в носу бобра. Подобными нервами располагает и нос человека. Некоторые хирурги - в случае учащения сердечного ритма во время операции на открытом сердце - погружают лицо больного в холодную воду на время, достаточное для нормализации ритма.
3. Люксембургская фирма MDI выпустила установочную серию гибридного автомобиля, работающего на сжатом воздухе. Запас в 90 м3 воздуха, сжатого в резервуаре под давлением в 300 атмосфер, позволяет проехать 100 км, пропуская этот через четырёхцилиндровый пневматический двигатель. За городом, где экологическая обстановка не так напряжена, можно включить небольшой бензиновый двигатель, способный ещё и подкачивать воздух в резервуар. Кроме того, если пневматический автомобиль получит достаточно широкое распространение, воздушные компрессоры придётся поставить на бензоколонках.
Объяснение задания лабораторной работы.
П: На распечатанных листах индивидуально для каждого представлено подробное описание работы, таблица, расчетные формулы.
Необходимо для различных значений объема измерить давление с помощью двух приборов: манометра и барометра. Напомним принцип их действия. (Краткие доклады двух студентов об устройстве и принципе действия манометра и барометра.)
Физическая минутка.
П: Чтобы немного отдохнуть, я предлагаю вам поиграть.
Игра в ассоциации по теме «физика» со всеми участниками занятия с помощью воздушного шарика. Шарик передается по кругу, при этом называют первую ассоциацию со словом «физика», начиная с преподавателя.
Инструктаж по технике безопасности.
П: Перед тем, как вы приступите к выполнению лабораторной работы, напоминаю вам правила безопасности при работе с приборами. Инструкция находится на ваших столах, прошу обратить внимание на пункты 1, 2, 3, 4, 6, 7, 16, 22 и 23.
Перед выполнением работы внимательно ознакомьтесь с ее содержанием. Как говорил всем известный ученый физик А. Эйнштейн: «Все что мы знаем о реальности, исходит из опыта и завершается им».
Можете приступать к измерениям.
Проведения опыта и оформление отчета.
Студенты, разделенные на две микрогруппы, выполняют опыт и вычисляют по результатам измерений необходимые величины, параллельно готовят устно вывод.
Формулировка вывода.
П: Вы провели опыт и определили постоянную величину с = PV, к каким выводам вы пришли?
Студенты дают свои варианты выводов по работе.
П: Давайте выберем наиболее предпочтительный вариант вывода по работе из представленных. (Варианты выводов на слайде.)
В ходе лабораторной работы мы на опыте проверили справедливость закона Бойля-Мариотта.
В ходе лабораторной работы мы вычислили постоянную величину с =….
Входе лабораторной работы мы вычислили величину с = … с относительной погрешностью …, которая по результатам оказалась постоянной для всех трех опытов, что доказывает справедливость закона Бойля-Мариотта.
В ходе лабораторной работы мы рассмотрели закон Бойля-Мариотта и вычислили постоянную величину с = … с относительной погрешностью ….
Формулировка темы лабораторной работы.
П: Уважаемые студенты, а вы не заметили ничего необычного в методических указаниях лабораторной работы. Верно, там не сформулирована тема нашей лабораторной работы. Сформулируем и запишем ее.
Рефлексия изученного материала.
П: Предлагаю подвести итог нашего занятия в творческой форме.
Творческое задание:
Составить синквейн о законе. (первая микрогруппа)
Существительное закон Бойля-Мариотта
Два глагола характеризует, объясняет
Три прилагательных газовый, изотермический, практичный
Главная мысль при постоянной температуре, произведение давления на объем также постоянно
Синоним первого существительного постановление
Заполнить паспорт закона. (вторая микрогруппа)
Имя Закон
Фамилия Бойль-Мариотт
Место рождения Англия, Франция
Пол мужской
Дата рождения 1662-1667гг.
Подведение итогов занятия.
П: На сегодняшнем занятии была проделана огромная работа по обобщению ваших знаний по теме газовые законы, вы выступили в роли экспериментаторов и проверили на опыте закон Бойля-Мариотта. Ваши отчеты в письменном виде я проверю к следующему занятию, ну а устный зачет вы все с блеском уже осуществили на протяжении всего занятия. Всем работа будем зачтена.
Рефлексия эмоционального состояния.
П: А теперь давайте посмотрим на кокой ноте мы заканчиваем наше сегодняшнее занятие. Снова обратимся к карточкам. Красный квадрат - «хуже не бывает», желтый – «так себе», зеленый - «отличное» (комментарии по результату).
Окончание занятия.
П: Благодарю вас за активную работу и внимание. Наше занятие окончено. До свидания.