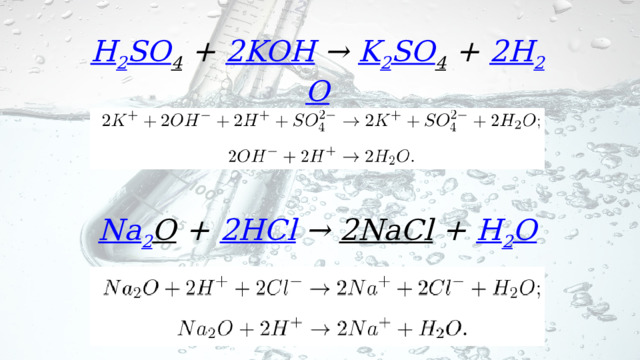Записать уравнения в молекулярном, полном и сокращенном ионном виде.
- KOH + H 2 SO 4 =
- HCl + Na 2 O=
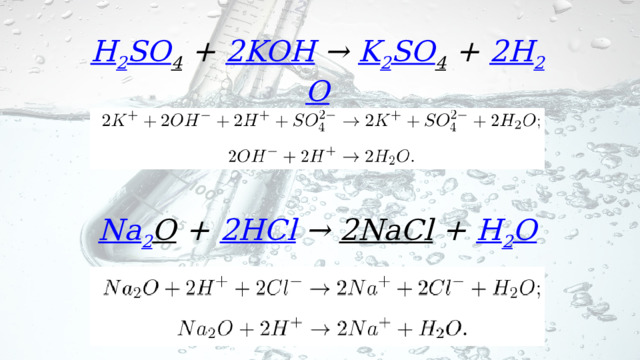
H 2 SO 4 + 2KOH → K 2 SO 4 + 2H 2 O
Na 2 O + 2HCl → 2NaCl + H 2 O

1. Al(OH) 3
2. HBr
4. OF 2
3. NH 4 Br
5. Cu(OH) 2
7. Cr 2 (SO 4 ) 3
6. КOH
8. H 2 SO 4
9. SO 3
Оксид
Двухосновная кислота
Щелочь
SO 3
H 2 SO 4
КOH


1 пробирка 2 пробирка 3 пробирка
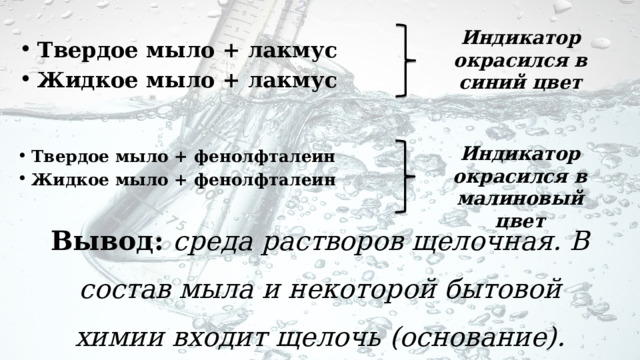
Индикатор окрасился в синий цвет
- Твердое мыло + лакмус
- Жидкое мыло + лакмус
Индикатор окрасился в малиновый цвет
- Твердое мыло + фенолфталеин
- Жидкое мыло + фенолфталеин
Вывод: среда растворов щелочная. В состав мыла и некоторой бытовой химии входит щелочь (основание).

Основания, их классификация и свойства. Способы получения оснований
Основания, ….

Определите основания
Основания
Ca(OH)2
CO
H 2 SO 4
КOH
HNO3
LiOH
NаOH
Al(NO3)3

Основание
это сложные вещества , в состав которых входят атомы металла, связанные с одной или несколькими гидроксогруппами (в зависимости от степени окисления металла)
это электролиты , которые при диссоциации образуют в качестве отрицательных ионов только гидроксид-анионы.

Напишите формулы
Формулы
Названия
Гидроксид натрия
Гидрокисд калия
Гидроксид кальция
Гидроксид железа (II)
NaOH
KOH
Ca(OH)2
Fe(OH)3

Основания
Запишите уравнения диссоциации веществ:
NaOH
Вa(OH)2
Fe(OH)3
+
Na +
OH -
2 OH -
Вa 2+
+
Не диссоциирует
Основаниями называют электролиты,
которые при диссоциации образуют
катионы металла и анионы гидроксогрупп ОН -

1 пробирка 2 пробирка 3 пробирка

Пробирка №3
Окраска индикатора не изменилась
- Fe(OH)3 + лакмус
- Fe(OH)3 + фенолфталеин
Вывод: окраска индикатора не изменяется в нерастворимых основаниях.

Третий лишний
Ba(OH) 2
1.КОН, NaOH, Ba(OH) 2
NH 4 OH
2.Са(ОН) 2 , Ba(OH) 2 , NH 4 OH
Fe(OH) 3
3.NaOH, Fe(OH) 3, Ba(OH) 2

Водный раствор аммиака

Работа с учебником
Рассмотрите таблицу 11 «Классификация оснований» на странице 243

растворимые
нерастворимые
сильные
слабые
однокислотные
двухкислотные
Основания
Гидроксид калия
Гидроксид натрия
Признак классификации
Количественно распад электролита на ионы
определяется степенью
диссоциации - = . 100%
Сильные электролиты 1
IА IIА
LiOH Ca(OH)2
NaOH Sr(OH)2
KOH Ba(OH)2
RbOH
CsOH
Слабые основания
0
Водный раствор аммиака
NH3 . H2O
Одно кислотные Двух кислотные
Li OH Mg (OH)2
Na OH Sr (OH)2
K OH Ba (OH)2
Rb OH Cu (OH)2
Гидроксид железа(III)
Гидроксид меди
n
N
Растворимость
в воде
Степень
эл.диссоциации
KOH
Едкое кали
NaOH
Едкий натр
Гидроксид кальция
Кислотность
Cu(OH)2
Fe(OH)3
Ca(OH)2
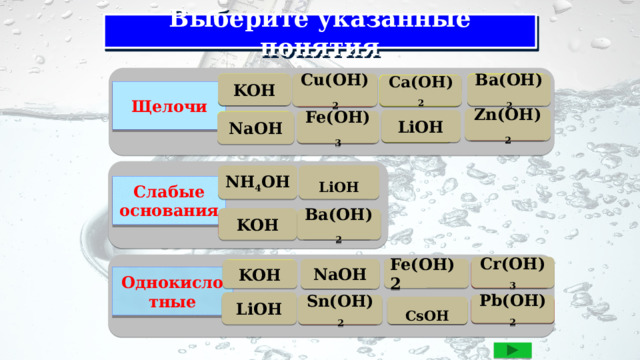
Выберите указанные понятия
KOH
Молодец
Cu(OH) 2
Молодец
Ошибка
Ba(OH) 2
Молодец
Ca(OH) 2
Щелочи
Zn(OH) 2
Ошибка
LiOH
Fe(OH) 3
Молодец
Молодец
NaOH
Ошибка
LiOH
NH 4 OH
Молодец
Ошибка
Слабые основания
KOH
Ошибка
Ba(OH) 2
Ошибка
Cr(OH) 3
Ошибка
Fe(OH)2
NaOH
Ошибка
Молодец
Молодец
KOH
Однокислотные
LiOH
Молодец
Sn(OH) 2
Pb(OH) 2
Ошибка
Ошибка
CsOH
Молодец

Домашнее задание
1.Прочитать параграф 40, составить схему «Классификация оснований»
2.Упр 2 стр 247
2.Используя Интернет-ресурсы, определите неизвестное основание. (текст домой)

Неизвестное основание
Это вещество способно разрушать органические вещества: бумагу, дерево, а также кожу человека, вызывая ожоги различной степени тяжести. В России оно зарегистрировано в качестве пищевой добавки Е- 524.
Некоторые традиционные блюда готовятся с применением этого вещества. Например, это скандинавское блюдо из рыбы под названием Лютефиск. Для его приготовления сушеная треска вымачивается 5-6 дней в этом веществе и приобретает из-за этого мягкую желеобразную консистенцию. Это вещество используется при производстве какао, карамели, мороженого, шоколада и лимонадов. О каком веществе идет речь?
Применение оснований
KOH
NaOH
LiOH
Ca(OH)2
Ba(OH)2

LiOH
Гидроксид лития
- электролит в щелочных аккумуляторах;
- поглотитель углекислого газа в противогазах, подводных лодках и космических кораблях;
- в стекольной и керамической промышленности.

KOH
Гидроксид калия
- В качестве пищевой добавки (Е525) (изготовлении какао, шоколада).
- Производство мыла и шампуней, отбеливателей.
- Электролит в щелочных батарейках.
- В строительстве: для изготовления штукатурки, гипсовых растворов, побелка.
- Для очистки сточных вод.

NaOH
Гидроксид натрия
- производство бумаги, картона
- Производство мыла, шампуня.
- Для изготовления
биодизельного топлива.
- Зарегистрирован в качестве
пищевой добавки E524.
- В гражданской обороне - для
дегазации и нейтрализации
отравляющих веществ.

Ca(OH)2
Гидроксид кальция
- Для приготовления известкового строительного раствора.
- Известковая вода. Для обнаружения углекислого газа.
При производстве сахара и приготовления смесей для борьбы с болезнями растений, побелки стволов.

Ba(OH)2
Гидроксид бария
- как реактив на SO 4 2− и CO 3 2− ( сульфат- и карбонат -ионы);
- Для очистки растительных
масел и животных жиров ;
- в нефтеперерабатывающей промышленности для производства присадок к маслам ;
- в производстве элементов питания постоянных источников тока.

Тест Химические свойства оснований
1.Тест включает в себя 10 вопросов.
2. Для начала работы перейдите к следующему слайду.
3.Выберите 1 правильный ответ из предложенных вариантов и щелкните по нему.
4.При правильном ответе появляется ,
при неправильном – .
5.Для перехода к следующему вопросу используйте кнопку
6.По окончании работы подсчитайте количество набранных баллов.
Инструкция
1.Нерастворимые в воде основания можно получить при взаимодействии:
7.Гидроксид кальция реагирует с
3.Взаимодействие между кислотными и основными оксидами относится к реакции:
9.В результате разложения гидроксида меди(II) образуются:
5.Реакцией нейтрализации называется реакция:
2.Какое из нижеприведенных свойств характерно только для нерастворимых в воде оснований:
6.Какой тип химической реакции не характерен для оснований:
10.С гидроксидом калия не реагирует :
8.В реакцию с раствором гидроксида натрия вступает каждое из двух веществ:
4.При какой реакции образуется нерастворимое основание:
Тест
Подсчитайте количество правильных ответов
0 - 5 баллов – оценка «2»
6 - 7 баллов – оценка «3»
8 - 9 баллов – оценка «4»
10 баллов – оценка «5»
А) металла с водой;
А) взаимодействие с кислотами;
А) реакция разложения;
А) металла с водой;
А) оксидом бария;
А) CuO и Ba(OH)2;
А) CuO и H2;
А) соединения;
А) кислоты с основным оксидом;
А) HNO3;
Б) взаимодействие с солями;
Б) оксида металла с водой;
Б) любого основного оксида с водой;
Б) P2O5 и H2SO4;
Б) Cu и H2O;
Б) замещения;
Б) кислоты с растворимым основанием;
Б) Cu2O;
Б) реакция замещения;
Б) хлоридом калия;
В) разложение при нагревании.
В) растворимой в воде соли данного
металла с щелочью.
В) щелочи с растворимой в воде солью.
В) H2S и Cu;
В) CuOH и H2;
В) CO2;
В) кислотного оксида с основным оксидом.
В) соляной кислотой;
В) обмена.
В) реакция обмена.
Г) H2S.
Г) CuO и H2O.
Г) HCl и H2.
Г) гидроксидом натрия.