| 2 | Целеполагание (слайд 3,4) | Организует подводящий к теме диалог. Учитель математики: Две науки – математика и химия призваны сегодня на урок, чтобы объединить свои усилия в решении практико-ориентированных задач, которые встречаются при подготовке к экзамену, как в химии, так и в математике. Учитель химии: проводит демонстрационный эксперимент по приготовлению растворов разной концентрации, который позволяет повторить основные понятия темы «раствор, растворитель, растворенное вещество, массовая доля» А также помогает ученикам сформулировать тему и цель урока. | Разбор проблемной ситуации для определения темы и постановки целей Наблюдают, анализируют демонстрационный эксперимент: Формулируют тему и задачи урока. Делают записи в маршрутных листах.
| Формирование УУД: Регулятивнвные: волевая саморегуляция в ситуации затруднения; учатся работать по предложенному учителем плану; определять и формулировать цель деятельности на уроке с помощью учителя. Коммуникативные: умение выражать свои мысли с достаточной полнотой и точностью; умение слушать и понимать речь других; учитывать разные мнения. Познавательные: умение ставить и формулировать проблему с помощью учителя |
| 3 | Повторение материала, актуализация знаний (слайд 5-13) | Учитель математики: Для урока необходимо повторить некоторые понятия, которые мы знаем в математике Устная разминка (математика): начнем с основных понятий: 1. Сотая часть числа называется …(процент) 2. Частное двух чисел называют …(отношение) 3. Верное равенство двух отношений называют …(пропорция) Давайте посчитаем (Письменная разминка): Математика: 1)Найти 20% от 6000 2)На сколько процентов число 110 меньше числа 550? 3) Найдите число, 40 % которого равны 24 Химия: 1)Что такое массовая доля растворенного вещества? (Отношение массы растворенного вещества к общей массе раствора.) 2)Какова формула для вычисления массовой доли растворенного вещества и производные от нее (w = m (р.в.)/m (р-ра ) ; m (р.в.)= m (р-ра) ×w ; m (р-ра) = m (р.в.)/ w ) 3)Что такое смеси? | 1)Повторяют пройденные понятия, на письменной разминке делают записи в маршрутных листах, производят расчеты, вспоминают формулы. 2)Производят самоконтроль | Формирование УУД: Регулятивные: оценка, контроль, коррекция |
| 4 | Основной этап. Решение практико-ориентированных задач (слайд 14-26) | 1)Ученикам предлагаются 3(по группам) практико-ориентированные задачи, которые в процессе профориентационного диалога с учениками выводят на градообразующие предприятия города Череповца ПАО «Северсталь», АО «Апатит», а далее на профессии, которым можно обучиться в СПО учреждениях нашего города и Вологодской области, а именно Череповецкий химико-технологический колледж, медицинский колледж и металлургический колледж. 2)Выполнение предложенных задач разными способами, химическим и математическим, практическая работа по решению задач 1 группа: При подкормках овощных и цветочных культур в почву вносится 200 г азота на 100 м2. Вычислите, сколько граммов аммиачной селитры надо внести на земельный участок площадью 10 м2. Запишите число с точностью до целых. 2 группа В реанимацию попадают больные, потерявшие много крови. В этих случаях используют 0,9 %-й раствор поваренной соли (ϸ= 1 г/мл), который называется физиологическим раствором. Задание: Представьте, что вы медсестра (медбрат) реанимационного отделения и должны срочно приготовить 200 мл такого раствора. Как вы на месте медсестры приготовили бы такой раствор? 3 группа Сплавили два слитка. Первый весил 105 г и содержал 40 % железа, второй весил 75 г и содержал 64% железа. Какой процент железа содержится в получившемся сплаве? Решите задачу двумя способами, по формулам, как в химии и математическим способом
| 1)Принимают участие в диалоге о предприятиях и профессиях, знакомятся со средними профессиональными учреждениями города и области, профессиями. 2)Работают в группах, находят практическое применение той или иной задачи, делают записи в маршрутном листе. 3)Делают выводы в выборе решения той или иной задачи, решают ее 1 группа: Первый способ (пропорция) NH4NO3 аммиачная селитра (нитрат аммония) 1) Найдем относительную молекулярную массу NH4NO3 (обратите внимание в формуле два атома азота). Mr (NH4NO3) = 14*2 + 4*1+ 3*16 = 80 2) Найдем массу нитрата аммония (аммиачной селитры), в которой содержится 200 г азота 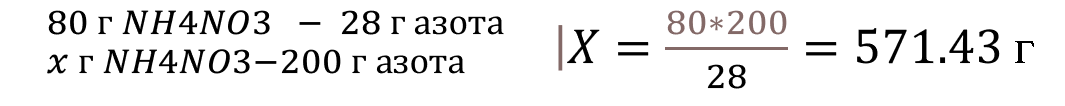 Мы ответили на вопрос задачи. Ответ просят привести с точностью до целых. Ответ: 571 г. Мы ответили на вопрос задачи. Ответ просят привести с точностью до целых. Ответ: 571 г. Второй способ (по формулам)  2 группа Дано: М(раствора)=200 мл P(NaCl)=1 г/мл W(NaCl)=0,09% Найти: m(NaCl)-? m(Н2О)-? Решение: m= P*V m раствора =200*1=200г. m(NaCl)=0,009*200=18г. m(Н2О)=200-18=182г. V(Н2О)=182 мл. Далее выполняют практическую часть на основе правил ТБ, делают соответствующие записи в маршрутных листах. 3 группа Решают задачу двумя способами: по формулам и знакомятся с методом стаканчиков (пояснения учителя) и составляем уравнение реакций: 0,4*105+0,64*75=180*0,01х 42+48=1,8х 1,8х=90 Х=50 Ответ: 50%
| Формирование УУД: Развивающие: проговаривание последовательности действий на уроке; формирование познавательной инициативы. Познавательные: умение находить и выделять необходимую информацию; умение делать предположения и обосновывать приемы решения той или иной задачи. Умение применить математические расчеты для реализации практической части задачи. Личностные: умение осознавать ответственность за общее дело; умение следовать в поведении моральным нормам и этическим требованиям. Коммуникативные: умение выражать свои мысли с достаточной полнотой и точностью; умение слушать и понимать речь других; учитывать разные мнения |
| 5 | Закрепление материала (слайд 27) | Учитель химии: – Посмотрите на содержание всех решенных сегодня задач. Что их объединяет? (Задачи на растворы, сплавы) В каких профессиях можно применить полученные знания на уроке? – действительно, во всех задачах фигурируют водные растворы(сплавы); расчеты связаны с массовой долей растворенного вещества; -если вы обратили внимание, задачи касаются разных сторон нашей жизни, профессий металлурга, медработника, работника химического производства. Учитель математики: – Посмотрите на эти задачи с точки зрения математики. Что их объединяет? Давайте закрепим сегодняшний материал, решив небольшой тест с системе Online Test Pad (по ссылке) | Высказывают свое мнение о разных суждениях, способах решения задач в математике и химии Решают итоговый тест: https://onlinetestpad.com/cuv6ziw244ljg (тест самостоятельно создан авторами урока) производят самоконтроль 1)Найти 5% от 2000? 2)В сплаве содержание меди составляет 25%.Сколько меди содержится в сплаве массой 142 кг. 3) В растворе соли массой 150 г с массовой долей вещества 10% масса соли равна 4) Формула для определения массовой доли вещества 1.С = n/ V 2. ω = m(в-ва) * m(р-ра) 3. ω = m(в-ва) / m(р-ра) 5)Смесью веществ не является: 1.почва 2.воздух 3.вода дистиллированная | Формирование УУД: Регулятивные: оценка, контроль, коррекция Познавательные: оценивать новые знания, приобретенные во время участия в уроке, беседах. Коммуникативные: умение обсуждать результаты, давать оценку своей деятельности и деятельности одноклассников; высказывать свое мнение. Личностные: высказывают свои мнения, чувства, личностную значимость участия в играх. |
| 6 | Рефлексия, подведение итогов (слайд 29) | Полезным ли для вас оказался этот интегрированный урок? Смогли ли вы выбрать наиболее подходящий для вас способ решения? Будете ли вы использовать эти методы в дальнейшем и при решении задач? Учитель химии: Сканируйте QR код с экрана и оцените урок и себя на уроке Наш урок подошел к концу. Спасибо за урок! | Высказывают свое мнение в диалоге, Сканируйте QR и производят рефлексию 
| Формирование УУД: Личностные: умение оценивать себя на основе критерия успешности. Познавательные: умение контролировать и оценивать процесс и результаты деятельности. Коммуникативные: умение выражать свои мысли с достаточной полнотой и точностью; умение слушать и понимать речь других. |







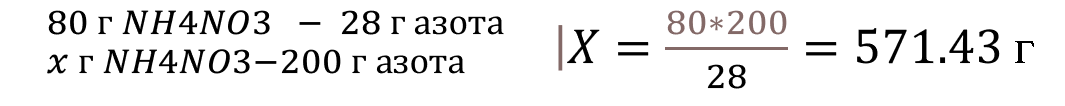 Мы ответили на вопрос задачи. Ответ просят привести с точностью до целых. Ответ: 571 г.
Мы ответили на вопрос задачи. Ответ просят привести с точностью до целых. Ответ: 571 г.











