Просмотр содержимого документа
«Презентация к уроку химии "Химическая связь и ее виды"»

ХИМИЧЕСКАЯ СВЯЗЬ. ЕЁ ВИДЫ
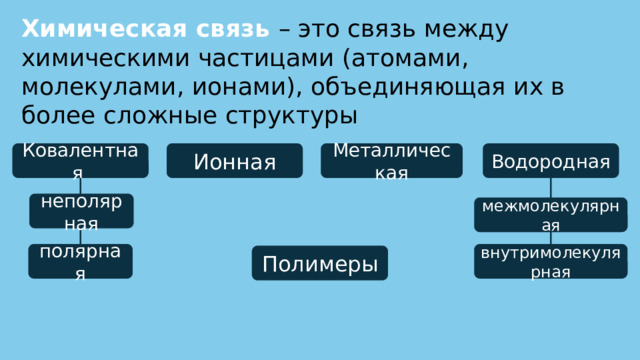
Химическая связь – это связь между химическими частицами (атомами, молекулами, ионами), объединяющая их в более сложные структуры
Ионная
Металлическая
Ковалентная
Водородная
неполярная
межмолекулярная
полярная
внутримолекулярная
Полимеры

Ковалентная
неполярная
- связь, которая образуется за счет общих электронных пар между атомами двух неметаллов, не отличающихся по электроотрицательности
Ковалентная
полярная
Ионная
H – H
Металлическая
O 2 , Br 2 , N 2
Водородная

Ковалентная
неполярная
- связь, которая образуется за счет общих электронных пар между атомами двух неметаллов, незначительно отличающихся по электроотрицательности
Ковалентная
полярная
Ионная
H Cl
Металлическая
NH 3 , HI, CO 2
Водородная

Ковалентная
Донорно-акцепторная связь
неполярная
образование ковалентной связи за счёт вакантной орбитали одной частицы и неподеленной электронной пары другой частицы.
Ковалентная
полярная
Ионная
Металлическая
Водородная

Ковалентная
неполярная
- связь, которая образуется за счет электростатического притяжения между катионами и анионами, в которые превращаются атомы или группы атомов в результате отдачи и присоединения электронов.
Ковалентная
полярная
Ионная
Металлическая
NaOH, CuSO 4 , K 3 N
Водородная

Ковалентная
неполярная
- связь в металлах и сплавах между атом – ионами, которая осуществляется совокупностью валентных электронов
Ковалентная
полярная
Ионная
Металлическая
Ag, Cu, Ca
Водородная

Ковалентная
неполярная
- связь, возникающая между атомами H одной молекулы и атомами наиболее электроотрицательных элементов ( F, O, N ) другой молекулы
Ковалентная
полярная
Ионная
Металлическая
H 2 O, HF, CH 3 OH, NH 3
Водородная
Ковалентная
неполярная
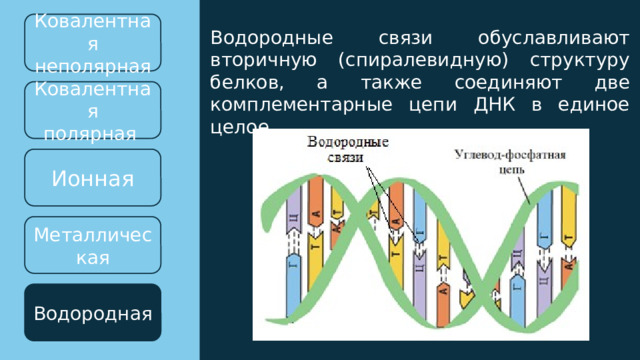
Водородные связи обуславливают вторичную (спиралевидную) структуру белков, а также соединяют две комплементарные цепи ДНК в единое целое.
Ковалентная
полярная
Ионная
Металлическая
Водородная
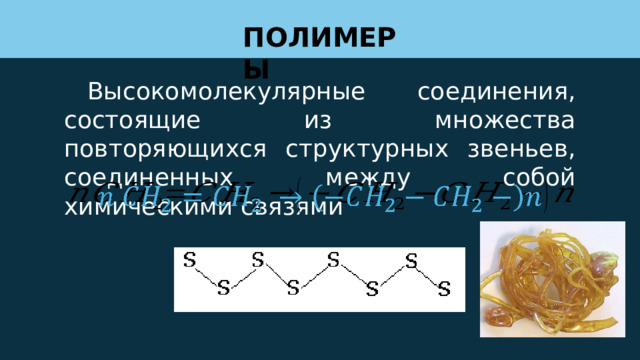
ПОЛИМЕРЫ
Высокомолекулярные соединения, состоящие из множества повторяющихся структурных звеньев, соединенных между собой химическими связями
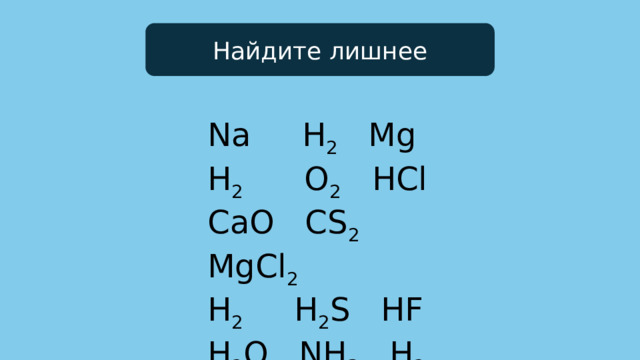
Найдите лишнее
Na H 2 Mg
H 2 O 2 HCl
CaO CS 2 MgCl 2
H 2 H 2 S HF
H 2 O NH 3 H 2

Типы химической связи
Распределить по колонкам
H 2 O, KF, Ag, NaI, O 2 , NaCl, Mo, NH 3 , Cd, N 2 , Cl 2 , CO 2 , LiBr, H 2 , H 2 S, Cu
Ковалентная неполярная
Ковалентная полярная
Ионная
Металлическая
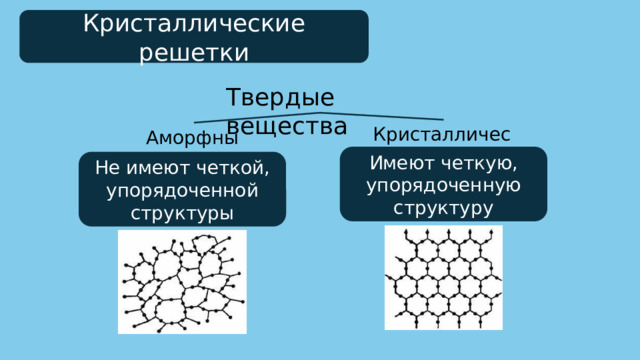
Кристаллические решетки
Твердые вещества
Кристаллические
Аморфные
Имеют четкую, упорядоченную структуру
Не имеют четкой, упорядоченной структуры

КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА –
совокупность точек пространства, в которых располагаются частицы, образуя кристалл

Кристаллические решетки
Молекулярные
Металлические
Атомные
Ионные
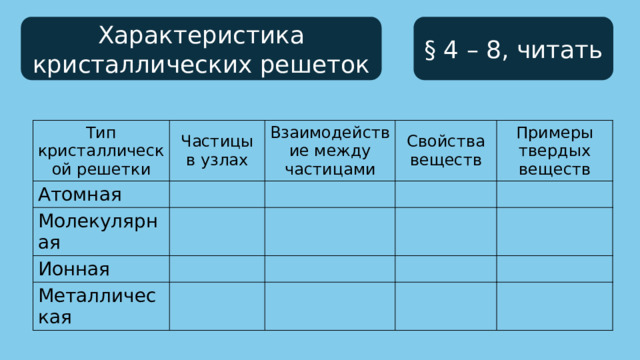
§ 4 – 8, читать
Характеристика кристаллических решеток
Тип кристаллической решетки
Частицы в узлах
Атомная
Взаимодействие между частицами
Молекулярная
Свойства веществ
Ионная
Примеры твердых веществ
Металлическая

































