
Кислоты в свете теории электролитической диссоциации
Подготовила преподаватель химии и биологии ГБПОУ «Железноводский художественно-строительный техникум
имени казачьего генерала В.П. Бондарева» Королькова О.В.

Цели урока
- Вспомнить понятие о кислотах, как о классе электролитов;
- Рассмотреть классификацию кислот по различным признакам;
- Охарактеризовать общие свойства кислот в свете ионных представлений;
- Научиться пользоваться электрохимическим рядом напряжений металлов и таблицей
растворимости для
прогнозирования возможных
химических реакций;
План урока
- I . Состав и классификация кислот;
- II . Ионные уравнения реакций на примере химических свойств кислот;
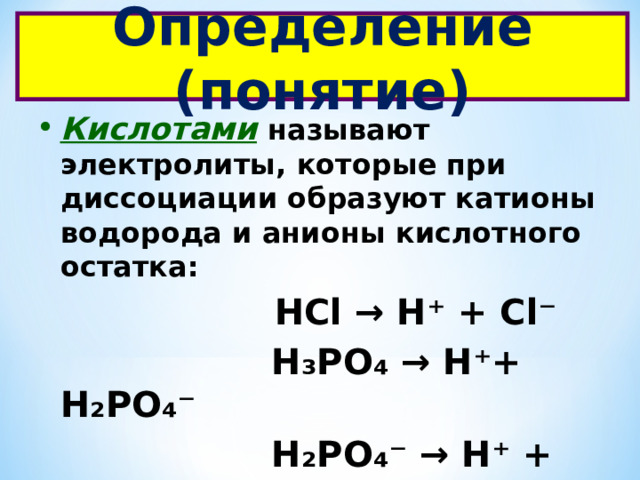
Определение (понятие)
- Кислотами называют электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка:
HCl → Н⁺ + С l⁻
Н₃РО₄ → Н⁺+ Н₂РО₄⁻
Н₂РО₄⁻ → Н⁺ + НРО₄²⁻
НРО₄²⁻ → Н⁺ + РО₄³⁻

Задание
формулы кислот:
К N О₂ Н₂О₂ Н₂СО₃
N аН S О₄ N аОН Н F
Са(ОН)₂ М g( НСО₃)₂ Н₂ S О₄ А l ( N О₃)₃
С u ОН НМ n О 4 ВаОНС l Р₂О₅ Н N О₂
Ответ
- К N О₂ Н₂О₂ Н₂СО₃ N аН S О₄ N аОН Н F Са(ОН)₂ М g( НСО₃)₂ Н₂ S О₄ А l ( N О₃)₃ С u ОН НМ n О 4 ВаОНС l Р₂О₅ Н N О₂

Кислоты бывают :
твердыми (фосфорная, кремниевая)
жидкими ( серная кислота).
Такие газы , как хлороводород HCl , бромоводород HBr , в водных растворах образуют соответствующие кислоты .
Угольная H 2 CO 3 и сернистая H 2 SO 3 кислоты существуют только в водных растворах.
Они легко разлагаются на соответствующий оксид и воду.

Водные растворы соляной, серной, фосфорной и ряда других кислот не имеют окраски.
Водные растворы хромовой кислоты H 2 CrO 4 , имеют желтую окраску, марганцевой кислоты HMnO 4 – малиновую.
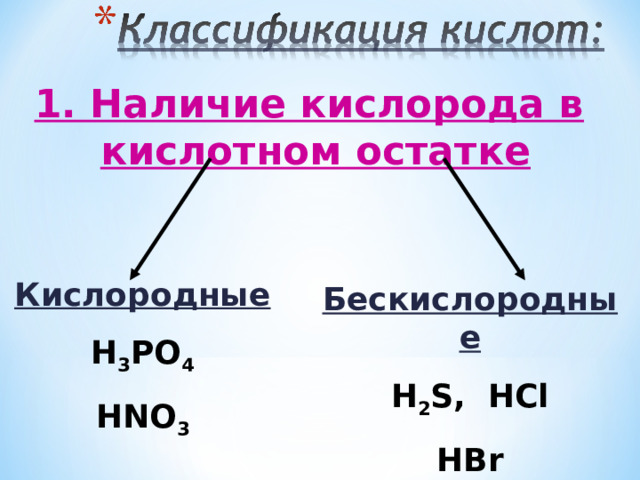
1. Наличие кислорода в кислотном остатке
Кислородные
H 3 PO 4
HNO 3
Бескислородные
H 2 S, HCl
HBr

2. Основность
(число атомов H в молекуле, способных замещаться на металл)
Одноосновные
HCl
HNO 3
Трёхосновные
H 3 PO 4
Двухосновные
H 2 S
H 2 SO 4
3. Растворимость в воде
Растворимые
H 2 SO 4
H 2 S
HNO 3
Нерастворимые
H 2 SiO 3

4. Летучесть
Нелетучие
H 2 SO 4
H 2 SiO 3
H 3 PO 4
Летучие
H 2 S
HCl
HNO 3

5. Степень электролитической диссоциации
Сильные
H 2 SO 4
HCl
HNO 3
Слабые
H 2 S
H 2 SO 3
H 2 CO 3

6. Стабильность
Нестабильные
H 2 SO 3
H 2 CO 3
H 2 SiO 3
Стабильные
H 2 SO 4
H 3 PO 4
HCl

Химические свойства кислот
кислота + основание → соль + вода
(реакция обмена)

- 2 N аОН + Н₂ S О₄ → N а₂ S О₄ + 2Н₂О
2 N а⁺ + 2ОН⁻ + 2Н⁺ + S О₄²⁻ → 2 N а⁺ + S О₄²⁻ + 2Н₂О
Н⁺ + ОН⁻ → Н₂О
- 3НС l + F е(ОН)₃↓ → F е Cl ₃ + 3Н₂О
3Н⁺ + 3С l ⁻ + F е(ОН)₃↓ → F е³⁺ + 3Cl ⁻ + 3Н₂О
3Н⁺ + F е(ОН)₃↓ → F е³⁺ + 3Н₂О
- Н₂ S О₄ + Ва(ОН)₂ → Ва S О₄↓ + 2Н₂О
2Н⁺ + S О₄²⁻ + Ва²⁺ + 2ОН⁻ → Ва S О₄↓ + 2Н₂О

- 2)Взаимодействие кислот с оксидами металлов:
кислота + оксид металла → соль + вода
(реакция обмена)
- С u О + Н₂ S О₄ → CuS О₄ + Н₂О
С u О + 2Н⁺ + S О₄²⁻ → Cu²⁺ + S О₄²⁻ + Н₂О
С u О + 2Н⁺ → ᵗ° Cu²⁺ + Н₂О
- F е₂О₃ + 6НС l → 2 F еС l ₃ + 3Н₂О
F е₂О₃ + 6Н⁺ + 6С l⁻ → 2 F е³⁺ + 6С l ⁻ + 3Н₂О
F е₂О₃ + 6Н⁺ → 2 F е³⁺ + 3Н₂О

- 3)Взаимодействие кислот с металлами:
кислота + металл → соль + водород
(реакция замещения)
- Условия протекания реакций:
1) Металл в электрохимическом ряду напряжений металлов должен находится до водорода:
Zn + 2НС l → ZnCl ₂ + Н₂↑
Zn 0 + 2 Н⁺ + 2С l⁻ → Zn ²⁺ + 2С l⁻ + Н₂ 0 ↑
Zn° + 2 Н⁺ → Zn ²⁺ + Н₂°↑
2) В результате реакции должна получиться растворимая соль: Pb + Н₂ S О₄ = Р bS О₄↓ + Н₂↑

- 3) Нерастворимые кислоты (кремневая) не вступают в реакции с металлами:
Н₂ Si О₃ + М g →
- 4) Концентрированный и разбавленный растворы серной кислоты,
а также раствор азотной
кислоты любой
концентрации
взаимодействую с
металлами по другой схеме.

- 3)Взаимодействие кислот с солями:
кислота + соль → новая кислота + новая соль
(реакция обмена)
- К₂СО₃ + 2Н N О₃ → 2К N О₃ + СО₂↑ + Н₂О
2К⁺ + СО₃²⁻ + 2Н⁺ + 2 N О₃⁻ → 2К ⁺ + 2 N О₃⁻ + СО₂ + Н₂О
СО₃²⁻ + 2Н⁺ → СО₂↑ + Н₂О
- СаСО₃↓ + 2НС l → СаС l ₂ + СО₂↑ + Н₂О
СаСО₃ + 2Н⁺ + 2С l ⁻ → Са² ⁺ + 2С l ⁻ + СО₂ + Н₂О
C аСО₃ + 2Н⁺ → Са²⁺ + СО₂↑ + Н₂О

Качественная реакция на S О₄² ⁻ ( сульфат-ион)
- ВаС l₂ + Н₂ S О₄ → Ва S О₄↓ + 2НС l
Ва²⁺ + 2 С l⁻ + 2 Н⁺ + S О₄²⁻ → Ва S О₄↓ + 2Н⁺ + 2 С l⁻
Ва²⁺ + S О₄²⁻ → Ва S О₄↓
- Сульфат бария (Ва S О₄ ) – белый осадок, не растворимый в азотной кислоте.
- Ва S О₄ + HNO 3 →

Качественная реакция на С l⁻ ( хлорид-ион)
- А gN О₃ + НС l → А gCl↓ + Н N О₃
А g⁺ + N О₃⁻ + Н⁺ + С l⁻ → А gCl↓ + Н⁺ + N О₃⁻
А g⁺ + С l⁻ → А gCl↓
- Хлорид серебра (А gCl) – белый творожистый осадок, не растворимый в азотной кислоте.

Итоги
кислот;
химические
свойства кислот;
- 3. Условия протекания типичных реакций кислот;

Закрепление
I вариант
II вариант
- Допишите уравнения реакций, отражающие химические свойства кислот:
- C какими из перечисленных веществ взаимодействует серная кислота. Составьте уравнения возможных реакции.
- HN О₃ + С u О →
- F е(ОН)₂ + НС l →
- H₂SO₄ + Mg →
- Н₃РО₄ + N аОН →
- SO₂ + H₂SiO₃ →
- НС l + MgO →
- C аСО₃ + Н N О₃ →
- Hg + НВ r →
- SiO₂ ;
- LiOH ;
- Ва( NO )₃;
- НС l ;
- К₂О;
- N а₂ Si О₃;
- Zn (ОН)₂
- LiNO₃ ;

Ответ
I вариант
II вариант
- HN О₃ + С u О → Cu ( NO₃ )₂ + Н₂О
- F е(ОН)₂↓ + 2НС l → FeCl₂ + 2 Н₂О
- H₂SO₄ + Mg → М gSO₄ + H₂↑
- Н₃РО₄ + 3N аОН → Na₃PO₄ + 3H₂O
- SO₂ + H₂SiO₃ →
- 2 НС l + MgO → MgCl₂ + H₂O
- C аСО₃ + 2 Н N О₃ → Ca ( NO₃ ) ₂ + СО₂ + Н₂О
- Hg + НВ r →
- Н₂ SO ₄ + SiO₂ →
- Н₂ SO ₄ + 2 Li ОН → Li₂SO₄ + 2H₂O
- Н₂ SO ₄ + Ba(NO₃)₂ → BaSO₄↓ + 2HNO₃
- Н₂ SO ₄ + HCl →
- Н₂ SO ₄ + K₂O → K₂SO₄ + H₂O
- Н₂ SO ₄ + Na₂SiO₃ → Na₂SO₄ + H₂SiO₃↓
- Н₂ SO ₄ + Zn(OH)₂ → ZnSO₄ + 2H₂O
- Н₂ SO ₄ + LiNO₃ →

Дополнительное задание
- Запишите молекулярные и ионные уравнения практически осуществимых реакций, протекающих между:
- магнием и соляной кислотой;
- оксидом бария и азотной кислотой;
- медью и фосфорной кислотой;
- нитратом калия и серной кислотой;
- оксидом лития и бромоводородной
кислотой;
- гидроксидом железа ( II ) и азотистой
кислотой;
- сульфитом натрия и соляной кислотой;

Ответ
Mg° + 2H⁺ + 2Cl⁻ → Mg²⁺ + 2Cl⁻ + H₂↑
Mg° + 2H⁺ → Mg²⁺ + H₂°↑
- BaO + 2HNO₃ → Ba(NO₃)₂ + H₂O
BaO + 2H⁺ + 2NO₃⁻ → Ba²⁺ +2NO₃⁻ + H₂O
BaO + 2H⁺ → Ba²⁺ + H₂O

- Li₂O + 2HBr → 2LiBr + H₂O
Li₂O + 2H⁺ + 2Br⁻ → 2Li⁺ + 2Br⁻ + H₂O
Li₂O + 2H⁺ → 2Li⁺ + H₂O
- Fe(OH)₂↓ + 2HNO₂ → Fe(NO₂)₂ + 2H₂O
Fe(OH)₂↓ + 2H⁺ + 2NO₂⁻ → Fe²⁺ + 2NO⁻ + 2H₂O
Fe(OH)₂↓ + 2H⁺ → Fe²⁺ + 2H₂O
- Na₂SO₃ + 2HCL → 2NaCl + SO₂↑ + H₂O
2Na⁺ + SO₃²⁻ + 2H⁺ + 2CL⁻ → 2Na⁺ + 2Cl⁻ + SO₂↑ + H₂O
SO₃²⁻ + 2H⁺ → SO₂↑ + H₂O













































