
Проверка домашнего задания (№2 стр 158)
2NaOH + Pb(NO 3 ) 2 = Pb(OH) 2 + 2NaNO 3
AlCl 3 +3КOH=Al(OH) 3 + 3KCl
Mg(NO 3 ) 2 +Ba(OH) 2 =Mg(OH) 2 + Ba(NO 3 ) 2
FeSO 4 +2NaOH=Fe(OH) 2 + Na 2 SO 4

Отгадайте загадки.
1.Два элемента в них всего-
Кислород важнее всего.
(оксиды)
2.Группы атомов о-аш -
Очень важный признак наш,
«Фенолфталеиновый» в нас
Становится малиновым.
(основания)

3.Водород в состав их входит,
За собой остаток водит,
Они кислые на вкус
Их ___________ зовут.
(кислотами)
4.Металл и кислотный остаток
В них дружно живут,
Эти вещества ______ зовут.
(солями)

Тема урока:
«Основные классы
неорганических соединений».

Девиз:
«Повторенье-мать
ученья».

Задание 1.
Допишите определения,
вставив пропущенные слова.

Оксиды – это сложные вещества, состоящие из _двух__ химических элементов, один из которых ___ кислород_ ____________ .
Основания – это __ сложные __ вещества, состоящие из атомов _ металла _____ , связанных с одной или несколькими __ гидроксогруппами –ОН .
Кислоты – это __ сложные в ещества, молекулы которых состоят из атомов водорода (Н) ___ и кислотного остатка ____ .
Соли – это сложные вещества, состоящие из атомов металла и кислотного остатка.

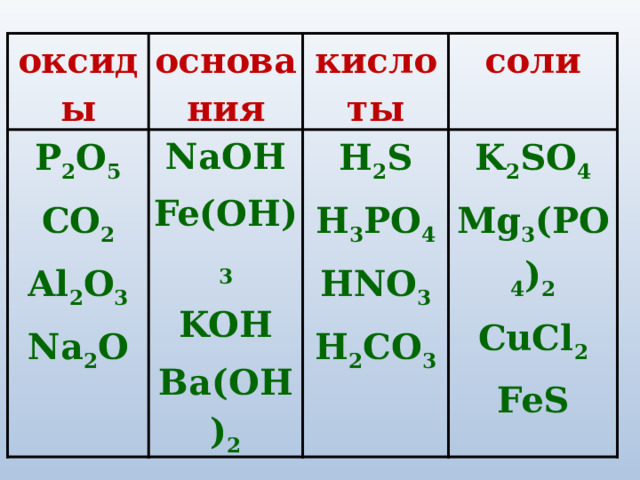
Задание 2.
Распределите по классам
следующие соединения:
H 2 S, P 2 O 5 , K 2 SO 4 , NaOH,
H 3 РO 4 , CO 2 , Fe(OH) 3 , Al 2 О 3 ,
Mg 3 (PO 4 ) 2 , KOH, HNO 3 , CuCl 2 ,
Ba(OH) 2 , Na 2 O, H 2 CO 3 , FeS.
оксиды
основания
P 2 O 5
кислоты
CO 2
NaOH
соли
H 2 S
Al 2 О 3
Fe(OH) 3
K 2 SO 4
H 3 РO 4
KOH
Na 2 O
Ba(OH) 2
HNO 3
Mg 3 (PO 4 ) 2
H 2 CO 3
CuCl 2
FeS

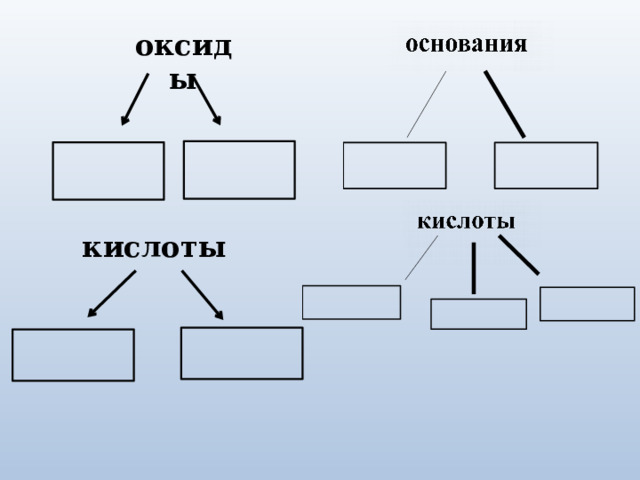
Задание 3.
Заполните схемы и
приведите примеры, используя
соединения из задания 2.
оксиды
кислоты
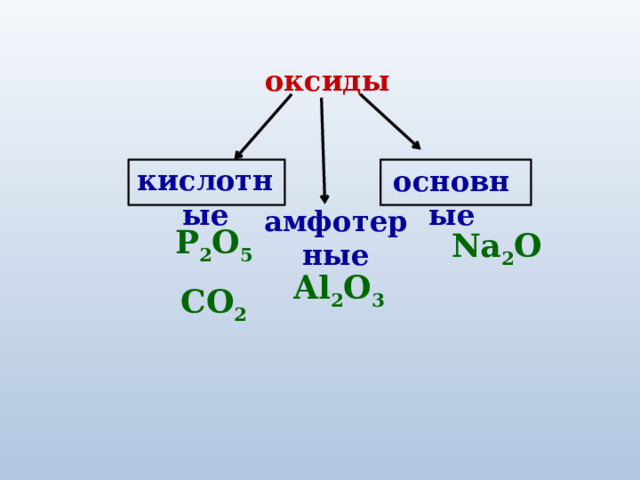
оксиды
кислотные
основные
амфотерные
P 2 O 5
CO 2
Na 2 O
Al 2 О 3
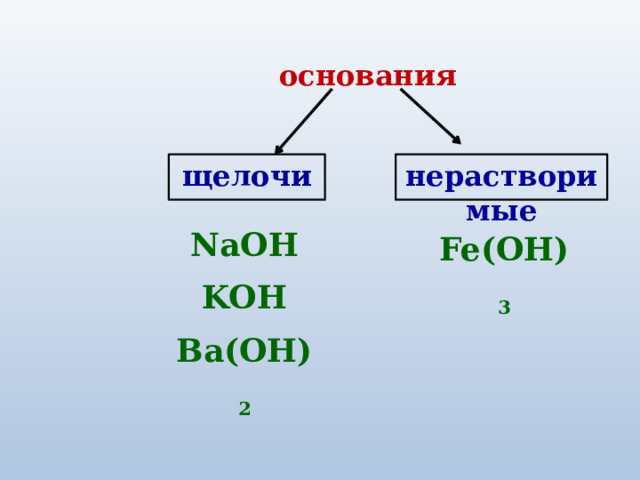
основания
щелочи
нерастворимые
NaOH
KOH
Ba(OH) 2
Fe(OH) 3
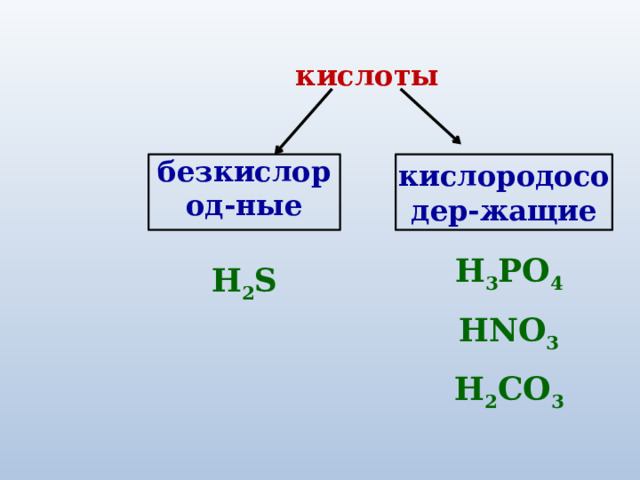
кислоты
безкислород-ные
кислородосодер-жащие
H 3 РO 4
HNO 3
H 2 CO 3
H 2 S
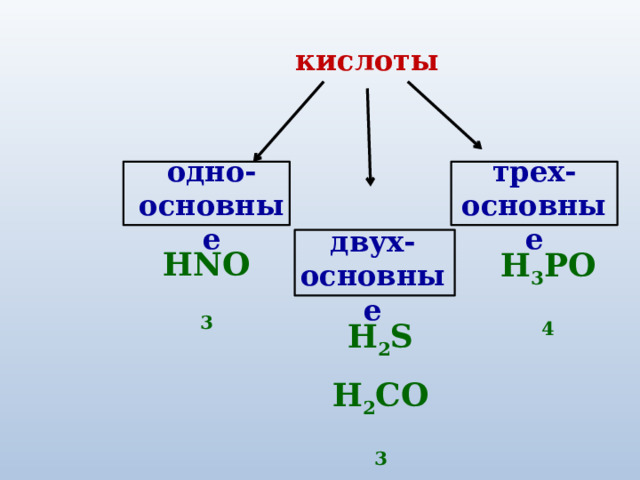
кислоты
одно-
трех-
основные
основные
двух-
основные
HNO 3
H 3 РO 4
H 2 S
H 2 CO 3
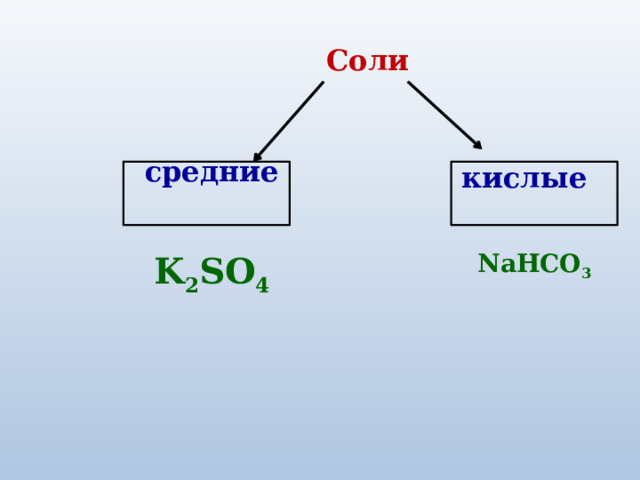
Соли
средние
кислые
K 2 SO 4
NaHCO 3

Задание 4.
Установите соответствие между
формулами соединений и их названиями.
Формулы
Названия
1. HCl
2. MgO
А . оксид серы (VI)
Б. гидроксид железа (III)
3. Al(NO 3 ) 3
В. кремниевая кислота
4. SO 3
Г. оксид магния
5. H 2 SiO 3
6. Fe(OH) 2
Д. гидроксид бария
Е. нитрат алюминия
7. Na 2 SO 3
8. Ba(OH) 2
Ж. гидроксид железа (II)
З. сульфат натрия
И. соляная кислота
К. сульфит натрия

Формулы
1. HCl
Названия
2. MgO
3. Al(NO 3 ) 3
И. соляная кислота
4. SO 3
Г. оксид магния
5. H 2 SiO 3
Е. нитрат алюминия
А. оксид серы (VI)
6. Fe(OH) 2
В. кремниевая кислота
7. Na 2 SO 3
8. Ba(OH) 2
Ж. гидроксид железа (II)
К. сульфит натрия
Д. гидроксид бария
1
2
И
3
Г
4
Е
5
А
6
В
7
Ж
8
К
Д
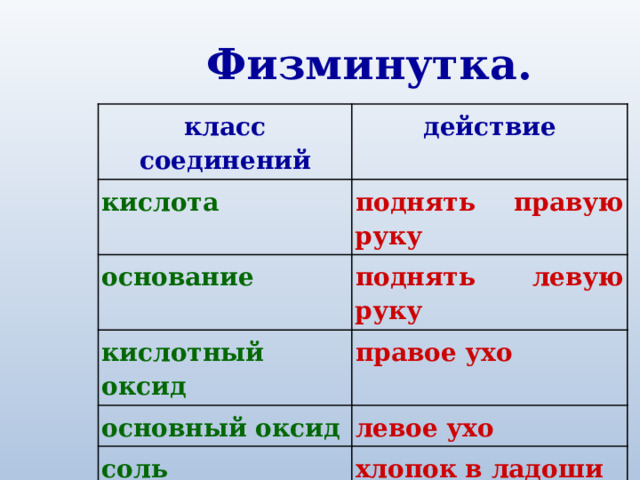
Физминутка.
класс соединений
действие
кислота
поднять правую руку
основание
поднять левую руку
кислотный оксид
правое ухо
основный оксид
левое ухо
соль
хлопок в ладоши

Задание 5.
Практическая работа.
Техника безопасности:
работа с кислотами и щелочами.

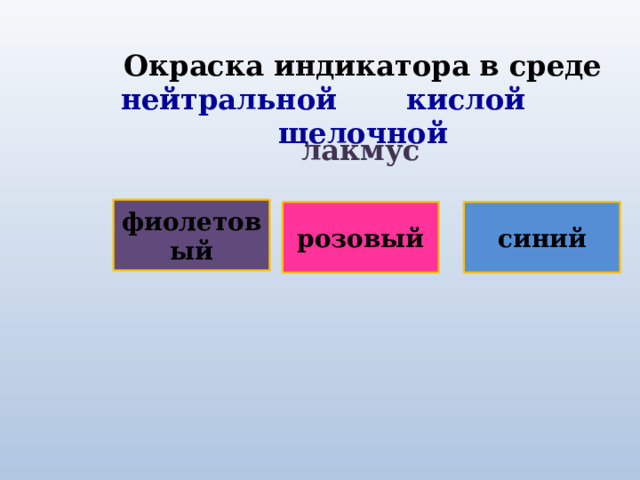
Окраска индикатора в среде
нейтральной кислой щелочной
лакмус
фиолетовый
розовый
синий

Пробирка №1 соль(средняя)
Пробирка № 2 – кислота
Пробирка № 3 - щелочь

Задание 6.
Допишите уравнения реакций, расставьте коэффициенты и укажите тип реакции.
Аl + НCl = АlCl 3 +
+ О 2 = МgО
Н 2 О + = H 2 SO 4
Сu(ОН) 2 + = СuCl 2 + Н 2 О
СаСО 3 = + СО 2
Н 2
2 6 2 3
Mg
2 2
SO 3
HCl
2 2
CaO

Задание 7.
Осуществите превращения и
дайте названия соединениям.
Mg → MgO → MgCl 2 → Mg(OH) 2 → MgO

Задание 8.
Решите задачу.
Рассчитайте массу оксида калия, необходимого для получения 37 г гидроксида калия.

Подготовиться к контрольной работе:
1)повторить § 30 – 37,
2)Выполнить задания из задачника контрольные вопросы по теме «Основные классы неорганических соединений» на с. 70-71(любой вариант на выбор.)
Домашнее задание.

Спасибо за урок!













































