Урок по химии в 10 классе
Тема: Фенолы.
Цель: изучить состав, строение, свойства фенола и его соединений.
Задачи:
Образовательные:
- на примере фенола конкретизировать знания учащихся об особенностях строения веществ, принадлежащих к классу фенолы,
- рассмотреть зависимость взаимного влияния атомов в молекуле фенола на его свойства
- познакомить учащихся с физическими свойствами фенола
- рассмотреть нахождение в природе, применение фенола и его соединений, их биологическую роль.
Развивающие задачи:
-совершенствовать умение учащихся прогнозировать свойства вещества на основе его строения
- продолжать развивать умение наблюдать, анализировать, делать выводы.
Воспитательные задачи:
- продолжить формирование химической картины мира через химическую картину природы (познаваемость, управление химическими процессами)
- расширить представление учащихся о влиянии фенолсодержащих промышленных отходов и строительных материалов на окружающую среду и здоровье человека
- рассмотреть биологическую роль фенола и его соединений на организм человека (положительную и отрицательную)
Тип урока: урок - изучения новых знаний
Методы обучения: словесный, наглядный
Ход урока:
1.Организационный момент (постановка цели и задач урока)
2.Актуализация знаний
1.Назовите органические вещества и определите к какому классу относятся? Слайд
2. Назовите какие функциональные группы входят в эту молекулу? ОН-группа и бензольное кольцо. Это фенолы. Таким образом, дайте определение Фенолам. (ученики сами дают определение Фенолам)
3.Изучение нового материала
1. Тема урока: Фенолы
2. Почему Фенолы представляют в отдельный класс, хотя также содержат ОН-группу как и спирты, или же бензольное кольцо как и арены?
Вспомним теорию Бутлерова. О чем гласят положения этой теории? Верно, согласно одного из положений теории Бутлерова, которое гласит, что свойства органических соединений зависят не только от состава вещества и порядка соединения атомов в молекуле, но и от взаимного влияния атомов и групп атомов друг на друга. Причем, наибольшее влияние оказывают атомы непосредственно связанные друг с другом.
Определение фенолов
Производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны непосредственно с бензольным кольцом, называются фенолами.
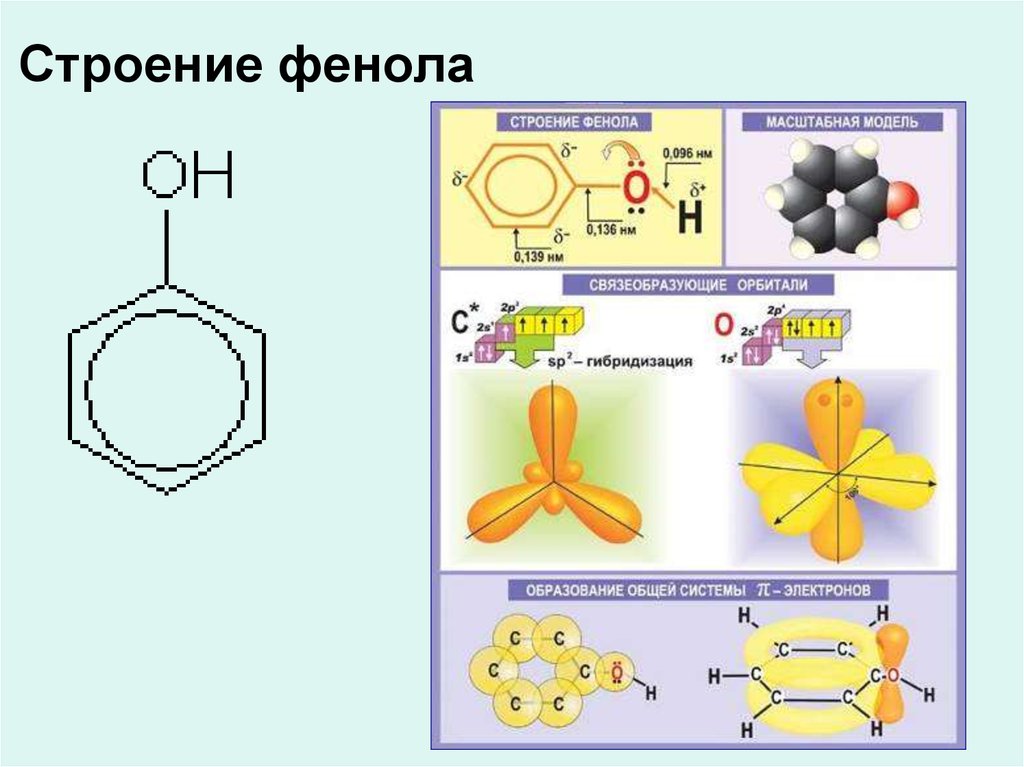
Строение молекулы фенола
Вспомним строение бензольного кольца, который есть и в аренах и в фенолах.
Рассматриваем строение бензольного кольца (слайды)
| 
| - неподеленная электронная пара атома кислорода притягивается 6-ти электронным облаком бензольного кольца, из – за чего связь О–Н еще сильнее поляризуется. Фенол - более сильная кислота, чем вода и спирты. - В бензольном кольце нарушается симметричность электронного облака, электронная плотность повышается в положении 2, 4, 6. Это делает более реакционноспособными связи С-Н в положениях 2, 4, 6. и – связи бензольного кольца. |
Рассмотрим влияние строения на химические свойства фенола в сравнении со спиртами

а) Рассмотрим реакции фенола по ОН- группе:
Кислотные свойства у фенола выражены сильнее, чем у спирта С2Н5ОН. Фенол – слабая кислота (карболовая).
Рассмотрим влияние строения на химические свойства фенола в сравнении с бензолом

Реакции фенола по бензольному кольцу

Какой вывод о взаимном влиянии атомов в молекуле фенола можно сделать?
Фенильная группа C6H5 – и гидроксил –ОН взаимно влияют друг на друга.

Классификация и изомерия фенолов
В зависимости от числа ОН-групп различают одноатомные фенолы (например, вышеприведенные фенол и крезолы) и многоатомные. Среди многоатомных фенолов наиболее распространены двухатомные и трехатомные:
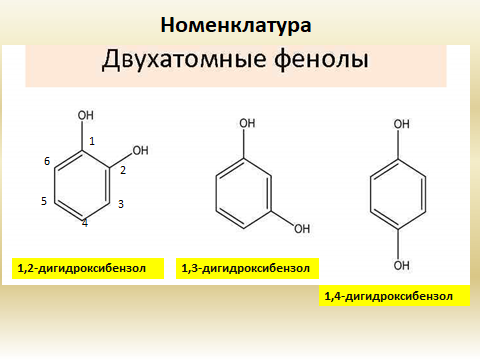

Как видно из приведенных примеров, фенолам свойственна структурная изомерия (изомерия положения гидроксигруппы).
Физические свойства фенола
Фенол представляет собой белые игольчатые кристаллы с характерным запахом, быстро розовеющие на воздухе в результате окисления. Он малорастворим в холодной воде, но неограниченно – в горячей.
температуры плавления у фенола (+43); температура кипения (+182).
Применение фенола
-для производства различного рода красителей, благодаря своему свойству изменять цвет в процессе окисления с бледно-розового до бурого оттенка.
–бактерицидное свойство: свойство фенола уничтожать бактерии и микроорганизмы, было взято на вооружение в кожевенном производстве при дублении шкур животных.
Позже фенол успешно использовался в медицине как одно из средств обеззараживания и дезинфекции хирургических инструментов и помещений, а в качестве 1,4-процентного водного раствора - как болеутоляющее и антисептик для внутреннего и наружного применения.
–для изготовления лекарств
– химическая промышленность, для изготовления пластмассы, фенолформальдегидных смол, таких искусственных волокон, как капрон и нейлон, а также различных антиоксидантов.
- для производства пластификаторов, присадок для масел, является одним из компонентов, входящих в состав препаратов по защите растений.
Физиологическое действие фенола.
Фенол - ядовит!!! При попадании на кожу вызывает ожоги, при этом он всасывается через кожу и вызывает отравление.
Биологическая роль соединений фенола:
| Положительная | Отрицательная (токсическое действие) |
| лекарственные препараты (пурген, парацетамол) антисептики (3-5 % раствор – карболовая кислота) эфирные масла (обладают сильными бактерицидными и противовирусными свойствами, стимулируют иммунную систему, повышают артериальное давление: - анетол в укропе, фенхеле, анисе - карвакрол и тимол в чабреце - эвгенол в гвоздике, базилике Флавоноиды (способствуют удалению радиоактивных элементов из организма) | фенолформальдегидные смолы пестициды, гербициды, инсектициды загрязнение вод фенольными отходами |
4. Закрепление нового материала (выполнение тестовых заданий)
Тест по теме « Фенолы»
1. Формула фенола:
А) С2Н5ОН Б) С6Н5ОН В) С6Н2Br3 Г) СН3СООН
2. Фенол проявляет:
А) кислотные свойства Б) основные свойства
В) амфотерные свойства Г) кислотно – основные свойства
3. Фенол – это
А) белое кристаллическое вещество, хорошо растворимо в холодной воде
Б) белое кристаллическое вещество, с характерным запахом, быстро розовеющее на воздухе вследствие окисления.
В) прозрачная жидкость с характерным запахом
Г) газообразное, ядовитое вещество
4. Фенол не получают из :
А) каменного угля Б) предельных углеводородов
В) бензола Г) изопропилбензола
5. Фенол не реагирует с:
А) NaOH Б) HNO3 B) H2O г) бромной водой
5. Домашнее задание.§13


























