Государственное автономное образовательное учреждение
среднего профессионального образования Республики Крым
«ЯЛТИНСКИЙ МЕДИЦИНСКИЙ КОЛЛЕДЖ»
I. Методический блок
Методическая разработка занятия
Тема: Растворы
Специальность ___33.02.01__________
Предмет______ОУП.13 ХИМИЯ___________
Курс__I_____ Семестр____I-II_____ Количество часов ____2___
Вид занятия: практическое занятие
1. Учебные цели: закрепить представления о растворении как физико-химическом процессе и растворах как физико-химических системах. Развивать навыки решения задач с использованием понятия «массовая доля растворенного вещества». Закрепить и углубить знания студентов об основных понятиях теории электролитической диссоциации (ТЭД), реакция ионного обмена, гидролиза солей.
Знать: понятие раствор, водородный показатель, сильные и слабые электролиты, массовая доля растворенного вещества, основные понятия теории электролитической диссоциации.
Уметь: классифицировать растворы по признаку растворимости, писать реакции электролитической диссоциации, определять водородный показатель, различать сильные и слабые электролиты, решать задачи с использованием понятия «массовая доля растворенного вещества».
2. Цели развития личности студента (воспитательные): воспитывать интереса к изучаемому предмету, творческое отношение к избранной профессии, формировать научное мировоззрение на примере изучения химии; воспитывать чувство взаимного уважения между студентами, чувство коллективизма и взаимопомощи; воспитывать у студентов профессиональное мышление, прививать тягу к фундаментальным наукам.
3. Активируемые ОК:
ОК 01. Выбирать способы решения задач профессиональной деятельности применительно к различным контекстам.
ОК 02. Использовать современные средства поиска, анализа и интерпретации информации, и информационные технологии для выполнения задач профессиональной деятельности.
ОК 04. Эффективно взаимодействовать и работать в коллективе и команде.
ОК 07. Содействовать сохранению окружающей среды, ресурсосбережению, применять знания об изменении климата, принципы бережливого производства, эффективно действовать в чрезвычайных ситуациях.
Междисциплинарная интеграция: ОУП.11 Биология, ОУП.12 Физика
4. Организационная структура урока
| № з/п
| Основные этапы занятия и их содержание
| Уровни усвоения знаний
| Методы обучения средства активизации | Материалы метод. и технического обеспечен.
|
| И 1. | Подготовительный этап Организация занятия
|
| Рапорт дежурного Заполнение журнала Проверка внешнего вида студентов |
| 2. | Обоснование актуальности темы
|
|
|
| 3. | Определение учебных целей
|
| см. п.2
|
| 4. | Мотивация учебной деятельности студентов |
|
|
| II 1.
2.
3. | Основной этап Актуализация знаний (контроль знаний, умений, навыков)
Изучение учебного материала по плану:
Физико-химические процессы в растворах Выполнение типовых заданий Лабораторное занятие
Закрепление и систематизация учебного материала |
II
II
II
II
| Устный фронтальный индивидуальн. опрос тестовый контроль
Устный фронтальный опрос
| Тесты вопросы дидактич. карточки
|
| III 1.
2.
3. | Заключительный этап Общие выводы
Ответы на возможные вопросы
Задание к самоподготовке
|
|
Учебная Литература, задание, вопрос |
|
| 4. | Домашнее задание |
| Габриелян О.С., Остроумов И.Г. Химия. стр. 47-60, 294-299, конспект
|
II. Информационный блок
Физико-химические процессы в растворах
Растворы — гомогенные (однородные) системы переменного состава, которые содержат два или несколько компонентов.
Массовой долей растворенного вещества называется отношение массы растворенного вещества к массе раствора:
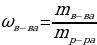 , где
, где
ω — массовая доля растворенного вещества, выраженная и долях единицы;
m(в-ва) — масса растворенного вещества, г;
m(р-ра) — масса раствора, г.
Массовую долю можно выражать также в процентах (%):
 , где
, где
Массовую долю растворенного вещества в процентах (%) часто называют процентной концентрацией раствора.
Молярную концентрацию можно рассчитать по формуле

На практике часто переходят от одного способа выражения концентрации к другому по известной плотности раствора, применяя формулу т = ρ • V.
Согласно теории электролитической диссоциации все реакции в водных растворах электролитов являются реакциями между ионами. Они называются ионными реакциями, а уравнения этих реакций - ионными уравнениями.
При составлении ионных уравнений реакций следует руководствоваться тем, что вещества малодиссоциированные, малорастворимые (выпадающие в осадок) и газообразные записываются в молекулярной форме.
Знак ↓, стоящий при формуле вещества, обозначает, что это вещество уходит из сферы реакции в виде осадка, знак ↑ обозначает, что вещество удаляется из сферы реакции в виде газа.
Сильные электролиты, как полностью диссоциированные, записывают в виде ионов. Сумма электрических зарядов левой части уравнения должна быть равна сумме электрических зарядов правой части.
В ВИДЕ ИОНОВ НЕ ЗАПИСЫВАЮТ:
1. Неэлектролиты (оксиды, простые вещества);
2. газы (H2S↑, NH3↑, SO2↑, CO2↑ );
3. осадки – нерастворимые и малорастворимые вещества (см. таблицу растворимости);
4. воду (как малодиссоциирующее вещество)
5. ИСКЛЮЧЕНИЕ: В таблице растворимости некоторые вещества указаны растворимы, но растворяются они только в закрытых сосудах, в открытых образуются газообразные вещества:
NH4OH → NH3↑ + H2O
H2SO3 → SO2↑ + H2O
H2CO3 → CO2↑ + H2O
Правила:
Простые вещества, оксиды, вода, газообразные вещества, а также нерастворимые кислоты, основания и соли не диссоциируют!
Для реакции берут растворы веществ, поэтому даже малорастворимые вещества находятся в растворах в виде ионов.
Если малорастворимое вещество образуется в результате реакции, то при записи ионного уравнения его считают нерастворимым.
Сумма электрических зарядов ионов в левой части уравнения должна быть равна сумме электрических зарядов ионов в правой части.
Гидролиз соли - это реакция обмена ионов некоторых солей с ионами воды.
С водой реагируют соли, образованные:
1) слабым основание и сильной кислотой,
2) сильным основанием и слабой кислотой.
Это объясняется тем, что в составе таких солей имеются ионы, которые могут связываться с ионами вода.
3) Еще легче подвергаются гидролизу соли, образованные слабым основанием и слабой кислотой
2. Типовые задания
Напишите уравнения химических реакций в молекулярном, полном ионном и сокращенном ионном виде:
1. гидрооксид меди +азотная кислота
2. нитрат свинца+иодид натрия
К 300 г 10%-го раствора гидроксида натрия добавили 60 г чистого гидроксида натрия. Вычислите массовую долю растворенного вещества в полученном растворе. Ответ укажите в процентах с точностью до целых
Растворяя соль в горячей воде, приготовили 200 г 55%-го раствора. При охлаждении раствора из него выпало 50 г осадка безводной соли. Вычислите массовую долю соли в растворе над осадком. Ответ дайте в процентах с точностью до целых.
Для веществ, приведенных в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л). Запишите номера веществ в порядке возрастания значения pH их водных растворов.
1. Гидрокарбонат натрия.
2. Сульфат магния.
3. Сульфат натрия.
4. Соляная кислота.
5. Для веществ, приведенных в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л). Запишите номера веществ в порядке возрастания значения pH их водных растворов.
1. Нитрат бария.
2. Карбонат натрия.
3. Серная кислота.
4. Сульфат железа (III).
Лабораторное занятие «Растворы»
Цель работы: приобретение навыков приготовления растворов различной концентрации из сухой соли.
С правилами по технике безопасности ознакомлен и обязуюсь выполнять.
Подпись студента:
Инструктаж провел, знания по технике безопасности проверил:

Опыт 1 Приготовление раствора хлорида натрия с заданной массовой долей соли (%).
Алгоритм приготовления определѐнного объѐма раствора с заданной процентной концентрацией:
1 Рассчитать массу хлорида натрия и воды необходимого для приготовления раствора.
2 Для расчетов использовать формулу расчета процентной концентрации:
3 Взвесить на весах рассчитанную навеску (1).
4 Перенести навеску соли в колбу (2).
5 Отмерить необходимое количество воды при помощи мерного цилиндра(3).
5 Прилить в колбу воды и перемешать стеклянной палочкой до полного
растворения соли(4-5).
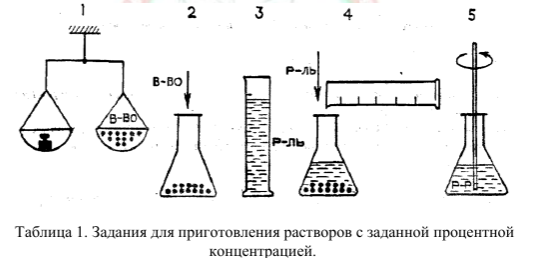
Таблица 1 Задания для приготовления растворов с заданной процентной
концентрацией.
| Вариант задания | Масса раствора | Процентная концентрация |
| 1 | 60 г | 2% |
| 2 | 120 г | 0,8% |
| 3 | 80 г | 2,5% |
| 4 | 140 г | 1,5% |
| 5 | 80 г | 3,5% |
| 6 | 140г | 1,25% |
| 7 | 160г | 0,6% |
| 8 | 90 г | 2,4% |
| 9 | 60г | 3,2% |
| 10 | 110 г | 3% |
Используя таблицу плотностей, рассчитайте молярную концентрацию, молярную концентрацию эквивалента и титр приготовленных вами растворов.
Таблица 2 Значения плотностей раствора хлорида натрия.
| Содержание NaCl |
| % | Плотность, г/мл |
| 0,6 | 1,0023 |
| 0,8 | 1,0036 |
| 1 | 1,0053 |
| 1,25 | 1,0068 |
| 1,5 | 1,0085 |
| 2 | 1,0125 |
| 2,4 | 1,0015 |
| 2,5 | 1,00158 |
| 3,2 | 1,0021 |
| 3 | 1,0195 |
Отчет о проделанной работе оформить в виде таблице.
| Заданная процентная концентрация раствора
| Заданная масса раствора
| Рассчитанные массы компонентов
| Плотность раствора
| Рассчитанный объем раствора
| концентрации |
| NaCl
| H2O
| См | Сн | Т |
|
|
|
|
|
|
|
|
|
|
3. Литература
Основная:
1. Габриелян О.С., Остроумов И.Г. Химия. Естественно-научный профиль: учеб. для студентов СПО. – М.: Образовательно-издательский центр «Академия», 2025. – 400с.
Дополнительная:
1. Габриелян О. С. Химия. Естественно- научный профиль. Книга для преподавателя: метод. пособие для учреждений сред. проф. образования / О.С.Габриелян, Г.Г. Лысова, И.Г. Остроумов. — М.: Образовательно-издательский центр «Академия», 2024. — 424 с.
2.Журин А.А., Заграничная Н.А. Химия: метапредметные результаты обучения.М.ВАКО.2014.
3. Еремин В.В., Кузьменко Н.Е., Химия. Углублённый уровень. 11 класс: учебник - М.: Дрофа ,2014
4. Интернет- ресурсы:
Библиотека МЭШ - СПО. Базовый и расширенный. Понятие о дисперсных системах. Растворы. Растворимость веществ в воде. (видеоматериал) https://uchebnik.mos.ru/material/bcee275b-38a3-4ddd-b3cb-570d663b750b?menuReferrer=catalogue
Библиотека МЭШ - СПО. Расширенный. Электролитическая диссоциация. Сильные и слабые электролиты (видеоматериал) https://uchebnik.mos.ru/material/44071921-687d-42fc-aad1-0f2193334947
Библиотека ЦОК, урок химии, 11 класс. Электролитическая диссоциация. Сильные и слабые электролиты. Степень диссоциации https://lesson.edu.ru/my-school/lesson/55f2a92a-10d2-4277-a23e-a8a0d946f8b8?backUrl=https://urok.apkpro.ru/&token=00d3c187bded0129a346af21affaa6a9e375b1c38cf3d61632acf9035c32a694
Библиотека ЦОК, урок химии, 11 класс. Понятие о дисперсных системах. Представление о коллоидных растворах https://lesson.edu.ru/my-school/lesson/fe9aed96-2ecf-4e2b-a79d-7503fa84d73e?backUrl=https://urok.apkpro.ru/&token=00d3c187bded0129a346af21affaa6a9e375b1c38cf3d61632acf9035c32a694
Библиотека ЦОК, урок химии, 11 класс. Истинные растворы. Насыщенные и ненасыщенные растворы, растворимость. Кристаллогидраты https://lesson.edu.ru/my-school/lesson/718c7235-5ae0-4f46-8622-ecc8762b96c6?backUrl=https://urok.apkpro.ru/&token=00d3c187bded0129a346af21affaa6a9e375b1c38cf3d61632acf9035c32a694
Библиотека ЦОК, урок химии, 11 класс. Способы выражения концентрации растворов: массовая доля вещества в растворе https://lesson.edu.ru/my-school/lesson/1460291b-5d5a-4d36-93ca-11832e3caf46?backUrl=https://urok.apkpro.ru/&token=00d3c187bded0129a346af21affaa6a9e375b1c38cf3d61632acf9035c32a694
Библиотека ЦОК, урок химии, 11 класс. Способы выражения концентрации растворов: молярная концентрация https://lesson.edu.ru/my-school/lesson/1460291b-5d5a-4d36-93ca-11832e3caf46?backUrl=https://urok.apkpro.ru/&token=00d3c187bded0129a346af21affaa6a9e375b1c38cf3d61632acf9035c32a694
Библиотека ЦОК, урок химии, 11 класс. Ионное произведение воды. Среда водных растворов: кислотная, щелочная, нейтральная. Водородный показатель (pH) раствора. Лабораторный опыт: определение среды растворов с помощью индикатора https://lesson.edu.ru/my-school/lesson/eb35bd40-0b14-49a0-b8a1-e9bedeb931c9?backUrl=https://urok.apkpro.ru/&token=00d3c187bded0129a346af21affaa6a9e375b1c38cf3d61632acf9035c32a694
Библиотека ЦОК, урок химии, 11 класс. Гидролиз солей. Реакции, протекающие в растворах электролитов https://lesson.edu.ru/my-school/lesson/97ae92e8-247b-4490-a9c9-743d092efa87?backUrl=https://urok.apkpro.ru/&token=00d3c187bded0129a346af21affaa6a9e375b1c38cf3d61632acf9035c32a694
Библиотека ЦОК, урок химии, 11 класс. Практическая работа № 3 по теме "Химические реакции в растворах электролитов" https://lesson.edu.ru/my-school/lesson/c9697fc4-c61e-4a5a-b297-3d2b2a638b0e?backUrl=https://urok.apkpro.ru/&token=00d3c187bded0129a346af21affaa6a9e375b1c38cf3d61632acf9035c32a694
Библиотека ЦОК, Видеотека школьных экспериментов. https://videoteka.apkpro.ru/chem Видеоопыт «Определение среды раствора с помощью индикатора»
Глоссарий
Растворы — гомогенные (однородные) системы переменного состава, которые содержат два или несколько компонентов.
Растворение — сложный физико-химический процесс, который включает несколько стадий:
Тепловой эффект растворения равен сумме тепловых эффектов физического и химического процессов. Физический процесс протекает с поглощением теплоты, химический — с выделением.
Сольваты — продукты переменного состава, которые образуются при химическом взаимодействии частиц растворенного вещества с молекулами растворителя.
Электролиты – вещества, растворы или расплавы которых проводят электрический ток.
Индикаторы — вещества, изменяющие свой цвет в зависимости от среды раствора.
Реакции ионного обмена – это реакции между ионами, образовавшимися в результате диссоциации электролитов.
III. Блок контроля знаний
Вопросы для активизации познавательной деятельности студентов при изучении нового материала
1. Дайте определение понятиям: вещество, реагент, химическая реакция, продукт реакции.
2. Что такое скорость химической реакции?
3. Какие факторы влияют на скорость химической реакции?
4. Что такое раствор, приведите примеры?
Вопросы для закрепления и систематизации полученных знаний
Что такое электролиты и неэлектролиты? Приведите соответствующие примеры.
Что такое кислоты, основания, соли с точки зрения теории электролитической диссоциации?
Правила составления РИО.
Какова роль молекул воды в процессе электролитической диссоциации?
Охарактеризуйте процессы, которые происходят при диссоциации веществ с ионной и с ковалентной полярной связью.
Сформулируйте основные положения теории электролитической диссоциации.
На чем основана классификация электролитов на сильные и слабые? Приведите примеры сильных и слабых электролитов.
Поясните, как степень диссоциации слабого электролита зависит от его концентрации.







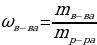 , где
, где , где
, где












