
Тема урока:

Цель : Расширить общее представление о явлении изомерии, рассмотреть ее виды. Формировать умение анализировать, сравнивать, устанавливать причинно – следственную связь. Развивать познавательный интерес на основе более глубокого осмысления сущности изомерии. Учить составлять формулы изомеров, называть их
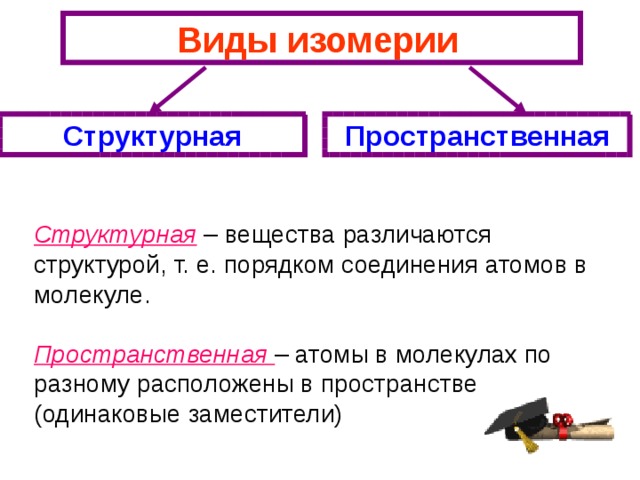
Виды изомерии
Структурная
Пространственная
Структурная – вещества различаются структурой, т. е. порядком соединения атомов в молекуле.
Пространственная – атомы в молекулах по разному расположены в пространстве (одинаковые заместители)

Т
И
П
Ы
С
Т
Р
У
К
Т
У
Р
Н
О
Й
И
З
О
М
Е
Р
И
И
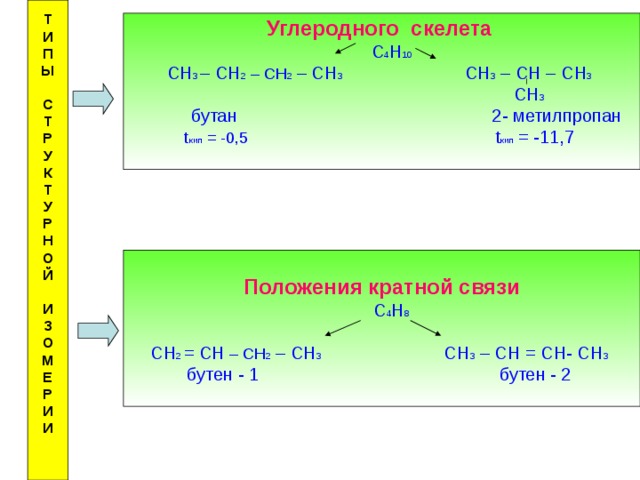
Углеродного скелета
С 4 Н 10
СН 3 – СН 2 – СН 2 – СН 3 СН 3 – СН – СН 3
СН 3
бутан 2- метилпропан
t кип = -0,5 t кип = -11,7
Положения кратной связи
С 4 Н 8
СН 2 = СН – СН 2 – СН 3 СН 3 – СН = СН- СН 3
бутен - 1 бутен - 2

Т
И
П
Ы
С
Т
Р
У
К
Т
У
Р
Н
О
Й
И
З
О
М
Е
Р
И
И
Положения функциональной группы
С 4 Н 10 О
СН 3 – СН 2 – СН 2 – ОН СН 3 – СН 2 – СН – СН 3
ОН
бутанол -1 бутанол - 2
Межклассовая
С 4 Н 10 О
СН 3 – СН 2 – СН 2 – СН 2 -ОН СН 3 – СН 2 – О - СН 2 - СН 3
бутанол - 1 диэтиловый эфир
С 4 Н 8
СН 2 = СН – СН 2 – СН 3 Н 2 С СН 2
Н 2 С СН 2
бутен – 1 циклобутан
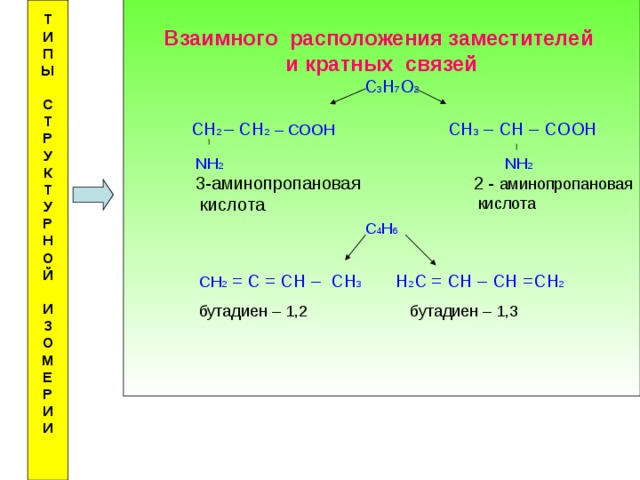
Взаимного расположения заместителей
и кратных связей
С 3 Н 7 О 2
СН 2 – СН 2 – СООН СН 3 – СН – СООН
С 4 Н 6
СН 2 = С = СН – СН 3 Н 2 С = СН – СН =СН 2
Т
И
П
Ы
С
Т
Р
У
К
Т
У
Р
Н
О
Й
И
З
О
М
Е
Р
И
И
NH 2
NH 2
3- аминопропановая
кислота
2 - аминопропановая
кислота
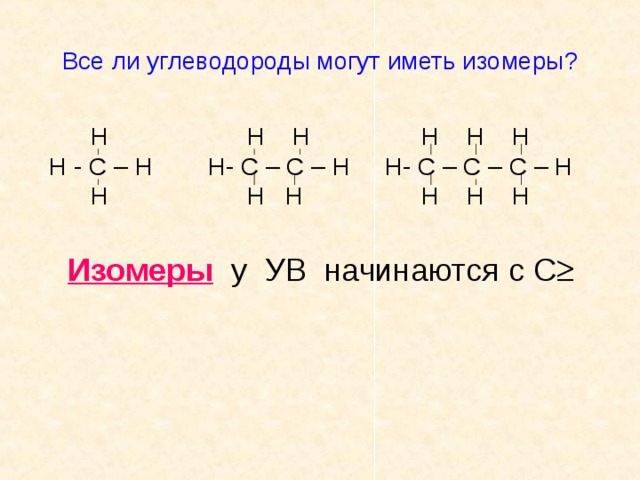
Все ли углеводороды могут иметь изомеры ?
Н Н Н Н Н Н
Н - С – Н Н- С – С – Н Н- С – С – С – Н
Н Н Н Н Н Н
Изомеры у УВ начинаются с С

По мере увеличения числа атомов углерода в молекуле У B число изомеров растет
У B формула
Метан
Число изомеров
СН 4
Этан
С 2 Н 6
1
Пропан
Бутан
1
С 3 Н 8
С 4 Н 10
1
Пентан
2
С 5 Н 12
Гексан
С 6 Н 14
3
Гептан
5
С 7 Н 16
октан
С 8 Н 18
9
18

Составьте структурные формулы возможных изомеров состава С 5 Н 12

Алгоритм составления структурных формул изомеров :
- Составить структурную формулу УВ с заданным
числом углеродных атомов
1 2 3 4 5
- С - С - С - С - С –
2. Затем постепенно укорачивать цепь (каждый раз
на один атом углерода) и производить всевозможные
перестановки одного или нескольких радикалов
(-СН 3 ) и таким образом вывести формулы изомеров
- с -
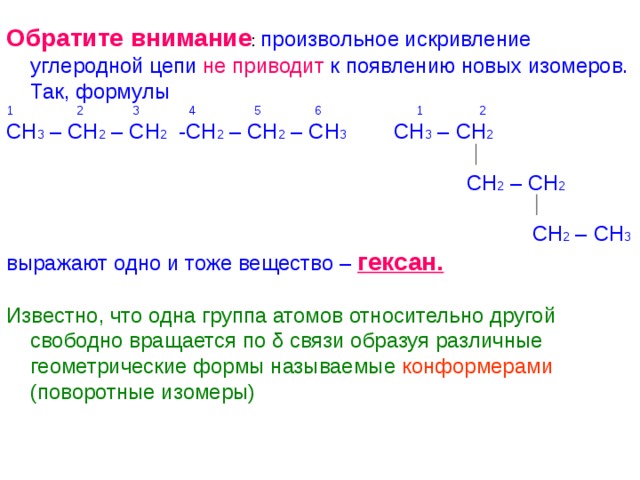
Обратите внимание : произвольное искривление углеродной цепи не приводит к появлению новых изомеров. Так, формулы
СН 3 – СН 2 – СН 2 -СН 2 – СН 2 – СН 3 СН 3 – СН 2
СН 2 – СН 2
СН 2 – СН 3
выражают одно и тоже вещество – гексан.
Известно, что одна группа атомов относительно другой свободно вращается по δ связи образуя различные геометрические формы называемые конформерами
(поворотные изомеры)


Возможно ли вращение одной атомной группы относительно другой ?

Пример : В результате вращения цепь может принять различные геометрические формы

Геометрические формы одной молекулы, образующиеся при вращении групп атомов вокруг сигма связей называют конформерами (или поворотными изомерами)
Обратите внимание : при образовании конформаций химическое строение остается неизменным (порядок связи атомов углерода)
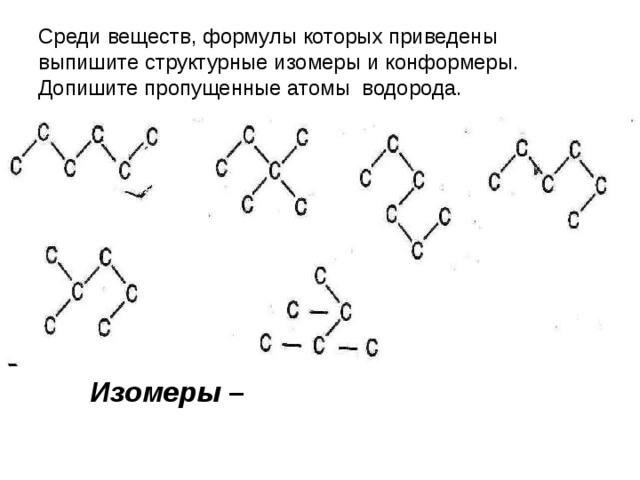
Среди веществ, формулы которых приведены выпишите структурные изомеры и конформеры. Допишите пропущенные атомы водорода.
Итак Изомеры – это вещества одного и того же состава, но разного строения
углеродной цепи
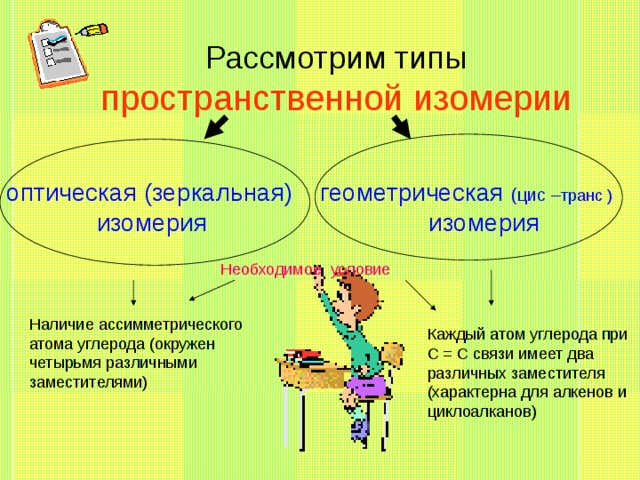
Рассмотрим типы
пространственной изомерии
оптическая (зеркальная) геометрическая (цис – транс )
изомерия изомерия
Необходимое условие
Наличие ассимметрического атома углерода (окружен четырьмя различными заместителями)
Каждый атом углерода при
С = С связи имеет два различных заместителя (характерна для алкенов и циклоалканов)
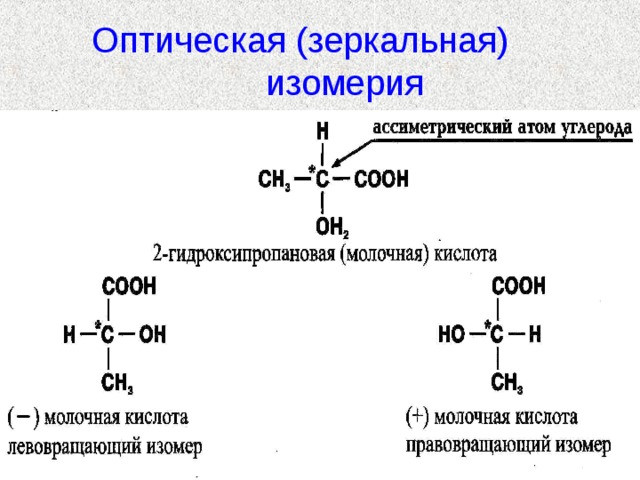
Оптическая (зеркальная) изомерия
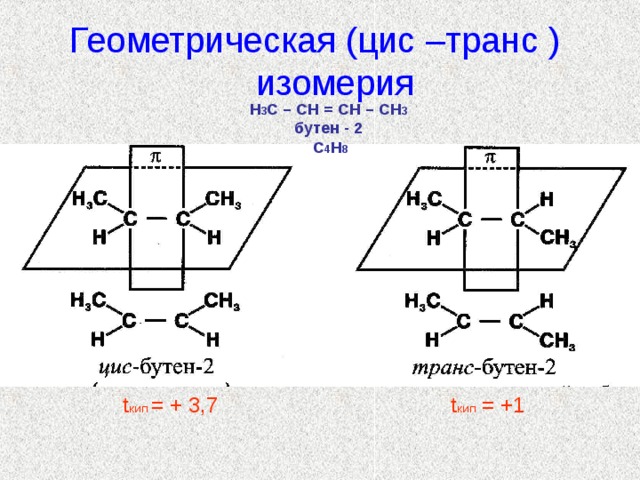
Геометрическая (цис –транс ) изомерия
Н 3 С – СН = СН – СН 3
бутен - 2
С 4 Н 8
t кип = + 3,7 t кип = +1
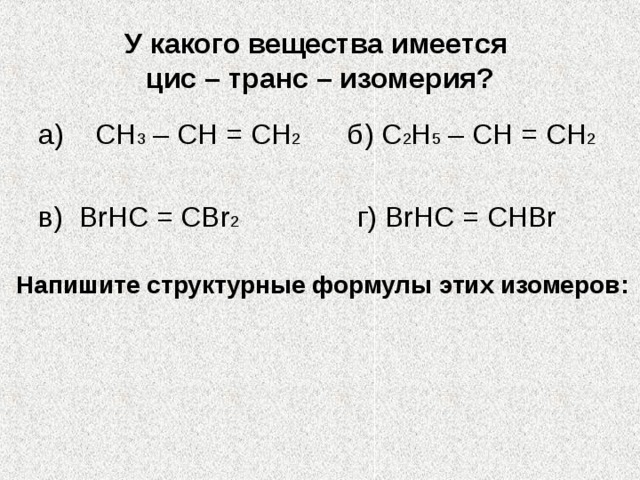
У какого вещества имеется цис – транс – изомерия ?
а) СН 3 – СН = СН 2 б) С 2 Н 5 – СН = СН 2
в) BrHC = CBr 2 г ) BrHC = CHBr
Напишите структурные формулы этих изомеров :

Ответы :
H H Br H
C = C C = C
Br Br H Br

УПРАЖНЕНИЕ № 5 стр. 42 учебник
СН 3 – СН – СН 2 – СН 3
ОН
Ответы
СН 3 СН 3
С С
Н Н
С 2 Н 5 ОН НО С 2 Н 5








































