8 класс
Учитель Красавина Е.Ф.
Тема урока: Кислоты
Цель урока: познакомиться с составом, классификацией и представителями кислот, развивать навыки экспериментировать, наблюдать, анализировать опыты.
Тип урока: изучение нового материала
Оборудование: лимонная кислота, уксусная кислота, индикаторы
Ход урока:
I Орг. момент
Вызов - пробуждение имеющихся знаний, интереса к полученной информации, актуализация жизненного опыта
Учитель:
Что нас объединяет?
Тема нашего урока зашифрована в шараде:
Мы первым слогом позовем кота,
Вторым измерим с судна толщу вод,
Союз на окончание пойдет,
И целым станет слово...
Ученики: Кислота.
Слайд 3 видео
Дождевая вода лишь на первый взгляд кажется чистой, не содержащей примесей. На самом деле в ней растворено немало веществ, например углекислый газ из атмосферы. Поэтому дождевая вода является слабым раствором угольной кислоты. После летней грозы в ней оказывается еще и азотная кислота, которая получается из оксидов азота, образующихся при горении воздуха вокруг пламенного шнура молнии, при работе реактивных двигателей самолетов и под воздействием солнечной радиации. Ежегодно с дождями на землю выпадает примерно 100 млн тонн азотной кислоты.
Немало кислот содержится и в нашей пище – фруктах, овощах, молочных продуктах, соусах, приправах, лекарствах. Ежедневно они поставляют в наш организм целый “букет” кислот: яблочную, щавелевую, уксусную, лимонную, аскорбиновую, винную, молочную, масляную. Синильная кислота, которая считается сильнейшим ядом, знакома каждому, кто разбивал косточки слив или вишен и лакомился их ядрышками. Так что ядрышками увлекаться не следует, особенно если они взяты из незрелых плодов.
Мы сталкиваемся с кислотами не только дома. Если летом в лесу присесть вблизи муравейника, то надолго запомнятся жгучие укусы его обитателей. Муравей не просто кусает, он впрыскивает в рану яд, содержащий до 70 % муравьиной кислоты. Из-за этой кислоты так жжется крапива. А тропический паук педипальпида, спасаясь от своих врагов, стреляет в них струйкой жидкости, состоящей на 84% из уксусной кислоты. “Химическое оружие” широко используется в природе, особенно в растительном царстве. Около 800 видов растений вырабатывают синильную кислоту и используют ее как оружие межвидовой борьбы.
Важна роль кислот в человеческом организме: например, аскорбиновая – поставщик витамина С. Аминокислоты образуют множество белков, а из них, в свою очередь, строятся все ткани нашего организма. “Много дел” и у соляной кислоты – сильнейшего бактерицида, под действием которого большинство бактерий, попавших в желудок, погибают.
Слайд 4-5 распространенность в природе, знакомство с серной кислотой (царица всех кислот, широкое применение кислоты), соляна кислота (значение для организма человека)
Слайд 6 обобщение опишите по картинкам пользу и вред кислот
II Изучение новой темы
Слайд 7
Внимательно посмотрите на формулы кислот. Что в них общего?
Слайд 8
Что такое кислота?
Давайте составим определение кислоты. ( Кислоты - это сложные вещества, состоящие из атомов водорода и кислотного остатка.
Слайд 9-12
Разделите вышеперечисленные кислоты на группы
1) по числу атомов водорода
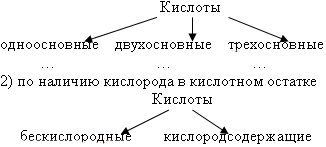
Слайд 13
Физические свойства кислот: демонстрация лимонной и уксусной кислот
Кислоты могут быть твердые, жидкие (разное агрегатное состояние),бесцветные, белые, коричневые (цвет разнообразный). Растворы имеют кислый вкус (яблочная , лимонная, щавелевая), растворимость (продемонстрировать растворимость лимонной кислоты), знакомство с таблицей растворимости (кремниевая кислота нерастворима), демонстрация минеральной газированной воды (неустойчивость угольной кислоты)
Слайд 14-15 видео «соляная кислота дымит» летучая
Слайд 16 учебник стр. 119 названия и формулы кислот (выучить)
Слайд 17 кислоты едкие вещества правила безопасности
Слайд 18 как определить в каком стаканчике вода, а в каком кислота? Качественные реакции действие индикаторов.
Слайд 19-20 техника безопасности. Лабораторный опыт. Инструкции на столе.
Слайд 21 закрепление материала, тест
Рефлексия
Домашнее задание


















