Первые попытки систематизации элементов
| 1829 г | Первую попытку систематизации элементов предпринимает немецкий химик Иоганн Вольфганг Дёберейнер 15.12.1780-24.03.1849. Ca-Sr- Ba; Li-Na-K; S-Se-Te; Cl-Br-I. В выделенных триадах элементов атомный вес среднего элемента триады примерно равен полусумме атомных весов двух крайних элементов. |
|
| Систематизация Гесса |
| 1862 | Александр Эмиль Бегуйе де Шанкуртуа (1820-1886)фр.ученый в г. предложил винтовой график элементов, расположенных в порядке возрастания атомных весов – т.н. "земная спираль" (vis tellurique). Винтовой график Шанкуртуа фиксирует закономерные отношения между атомными массами элементов, однако данная система не могла быть признана удовлетворительной. |
| 1864 г | Джон Александр Рейна Ньюлендс (1837-1898) анг. опубликует таблицу элементов, отражающую предложенный им закон октав. Ньюлендс показывает, что в ряду элементов, размещённых в порядке возрастания атомных весов, свойства восьмого элемента сходны со свойствами первого. Вследствие присущих системе Ньюлендса недостатков современники отнеслись к закону октав чрезвычайно скептически |
| 1864 г. | Немецкий ученый Мейер публикует первую таблицу, в которую включены 42 элемента (из 63), размещённые в шесть столбцов согласно их валентностям (в учебнике-1869) |
| 1870 г. | Выходит работа Мейера, содержащая новую таблицу и график зависимости атомного объёма элемента от атомного веса (массы) |
| 1869 г | закон периодичности свойств элементов Формулировка Менделеева Свойства простых тел, а также форма и свойства соединений химических элементов находятся в периодической зависимости от величины атомных весов (масс). Современная формулировка Свойства элементов, а также свойства простых веществ и сложных соединений этих элементов находятся в периодической зависимости от заряда их атомных ядер. |
|
| Полное научное объяснение периодическая система элементов Менделеева получила на основе квантовой механики. Закон и система Менделеева лежат в основе современного учения о строении вещества, играют первостепенную роль в изучении всего многообразия химических веществ и в синтезе новых элементов. |
Периодическая система элементов Менделеева, естественная система химических элементов, разработанная Д. И. Менделеевым на основе открытого им (1869) периодического закона-КОДЕКС ЭЛЕМЕНТОВ.
Периодическая система химических элементов- графическое выражение периодического закона.
Элементы систематизировались с учетом:
•свойств химических элементов
•атомных масс
•валентности

Известно около 600 видов таблицы Менделеева:
| короткопериодная –классическая таблица | длинная (полудлинная) длиннопериодная | самая длинная |
| Изучается в Азербайджане 
| рекомендована международным комитетом 
| 
|
Л естничная форма периодической системы элементов Д.И.Менделеева
естничная форма периодической системы элементов Д.И.Менделеева
http://www.theodoregray.com/PeriodicTable/Elements/RGBSamples/index.html
http://www.theodoregray.com/PeriodicTable/Collections.html
Периоды (dövrlər) -
Горизонтальные ряды (üfqi sıralar)-расположенные в порядке возрастания зарядов ядер атомов, начиная с щелочного металла(кроме первого периода) и заканчивая благородным газом
Номеруют периоды арабскими цифрами от1до 7(сверху вниз).
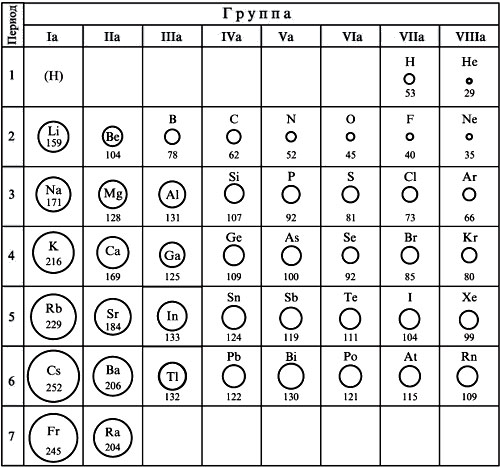
 1-3 малые периоды
1-3 малые периоды
4-7 – большие периоды
7 –незаконченный
(natamam dövr)
Три первых периода (горизонтальные ряды), состоящие каждый из одного ряда, называют малыми периодами.
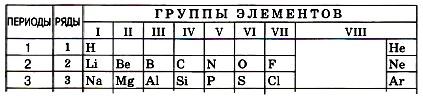
Периоды 4, 5 и 6-й (горизонтальные ряды) включают по два ряда элементов,их называют большими периодами;
4-й и 5-й периоды содержат по 18 элементов, 6-й — 32 элемента.

7-й большой период — незаконченный, состоит пока только из одного ряда.

В 6-м периоде после лантана см.*и в 7-м периоде после актиния см. ** расположены:.

В классической и в длинной форме периодической системы количество периодов совпадает.
В больших периодах короткой формы периодической системы имеется по два ряда.
В больших периодах длинной периодической системы- имеется по одному ряду т.е число рядов и в малых и больших периодах одинаковое – по одному .
В короткой форме периодической системы всего 10 рядов.
В длинной форме периодической системы число рядов равно количеству периодов =7 рядов(см. на след.листе).
В малых периодах расположены элементы главных подгрупп –А металлы и неметаллы
s- элементы – IA и II A и VIII A - He (гелий)
p- элементы - с III A по VIII A кроме He (гелий)
В короткой и в длинной форме периодической системы в малых периодах имеется по одному ряду
В больших периодах расположены:
| элементы главных подгрупп –А металлы и неметаллы s- элементы – IA и II A p- элементы - с III A по VIII A | элементы побочных подгрупп –В переходные металлы d – элементы I В по VIII В f –элементы I В по VIII В начиная с 6 периода (лантаноиды и актиноиды) |
Расположение типов элементов по периодам:
В 1-м — 2 элемента –неметаллы –водород и инертный газ -гелий (nəcib) təsirsiz qaz - s -элементы
во 2-м — 8 элементов- начинается с типичного металла (s –элемента) и заканчивается инертным газом (nəcib) təsirsiz qaz (p- элементом)
в 3-м — 8 элементов начинается с типичного металла (s –элемента) и заканчивается инертным газом (nəcib) təsirsiz qaz (p- элементом)
в 4-м — 18 элементов начинается с типичного металла(s –элемента, затем d – элементы ) и заканчивается инертным газом (nəcib) təsirsiz qaz (p- элементом)
в 5-м — 18 элементов начинается с типичного металла(s –элемента, затем d – элементы ) и заканчивается инертным газом (nəcib) təsirsiz qaz (p- элементом)
в 6-м — 32 элемента начинается с типичного металла (s –элемента, затем d и f – элементы) и заканчивается инертным газом (nəcib) təsirsiz qaz (p- элементом)
в 7-м —24 элемента начинается с типичного металла (s –элемента, затем d–элементы)
Известно всего 110 элементов.
Большинство элементов 7-го периода с тяжелыми ядрами например, америций (Z = 95) и последующие элементы не обнаружены в природе и получены искусственно - при ядерных реакциях, последние элементы этого периода еще не синтезированы,
У всех элементов одного периода одинаковое число электронных слоев (одинаковое главное квантовое число), равное номеру периода – «один этаж».
Некоторые элементы со сходными свойствами –ОБРАЗУЮТ СЕМЕЙСТВА:
с Z = 58-71 семейство — лантаноиды - f – элементы (6 период III B группа)
с Z = 90-103 семейство — актиноиды- f – элементы (7 период III B группа)

Длинная (полудлинная) форма периодической системы элементов Д.И.Менделеева
Группы – qruplar - Вертикальные столбцы элементов.
|
|
| I группа | | В | А | | 1 |
| Н | | 2 | 
| Li | | 3 |
| Na | | 4 |
| K | |
| Cu |
| | 5 |
| Rb | |
| Ag |
| | 6 |
| Cs | |
| Au |
| | 7 |
| Fr |
| В классической форме – 8 групп классической форме – 8 групп номеруют слева направо- (в длинной форме - 18 групп). Номер группы обозначается римскими цифрами I–VIII. В группах собраны элементы с одинаковым числом валентных электронов, количество которых, как правило, равно номеру группы.
Группы короткопериодной таблицы делятся на подгруппы: -главную (А) -побочную (В) (имеют разные типы валентных орбиталей: s- , p- , d , f). |
| Главные подгруппы(А) | Побочные подгруппы(В) |
| начинаются с 1 или 2 периода В группах А содержатся элементы -малых периодов -больших периодов Во всех группах одного периода имеется по одному элементу | начинаются с 4 периода В группах В содержатся элементы -только больших периодов Во всех группах одного периода имеется по одному элементу (кроме VIII В – имеется по 3 элемента) |
| Элементы I А -II А группы - s-элементы Гелий (Не) из VIII А группы - s-элемент Элементы IIIА-VIIIА группы(кроме гелия) - р-элементы | 1 В - VIII В группы - d – элементы III В группа 6 периода - f – элементы- лантаноиды III В группа 7 периода - f – элементы- актиноиды |
| Металлы, неметаллы и благородные газы | Только металлы |
Некоторые подгруппы А имеют обобщающее название
| Названия подгрупп А: | IА | щелочные металлы | s-элементы | литий, натрий, калий, рубидий, цезий, франций |
| IIА | щелочно-земельные металлы | s-элементы | кальций, стронций, барий, радий |
| IIIA | Семейство алюминия | р-элементы | алюминий, галлий, индий, таллий |
| I VA | Семейство углерода - | р-элементы | углерод, кремний, германий, олово, свинец |
| VA | пниктогены | р-элементы | Азот, фосфор, мышьяк, сурьма, висмут |
| VIA | халькогены | р-элементы | кислород, сера, селен, теллур, полоний |
| VIIA | галогены | р-элементы | фтор, хлор, бром, иод, астат |
| VIIIA | благородные, инертные газы | р-элементы (s-элемент – гелий) | гелий, неон, аргон, криптон, ксенон, радон |
Элементы одной и той же подгруппы и той же группы имеют сходные химические свойства(т.к. имеют одинаковое количество валентных электронов).
Например, группа АI:
| № | Характеристика элементов | Щелочные металлы |
| Li | Na | K | Rb | Cs |
| 1 | Агрегатное состояние (обычные условия) | Твердое |
|
| Общая электронная формула | …..пs1 |
|
| Число валентных электронов | 1 электрон на внешнем s- подуровне |
|
| Валентность | Постоянная |
| 2 | Высшие валентности в соединениях | Во всех соединениях валентность I |
| 3 | Гидриды RН | LiН | NaН | KН | RbН | CsН |
| 4 | Высшие оксиды R2О | Li2О | Na2О | K2О | Rb2О | Cs2О |
| 5 | Основания RОН | LiОН | NaОН | KОН | RbОН | CsОН |
| 6 | Карбонаты | Li2СО3 | Na2СО3 | K2СО3 | Rb2СО3 | Cs2СО3 |
| 7 | Нитраты | LiNО3 | NaNО3 | KNО3 | RbNО3 | CsNО3 |
| 8 | Ортофосфаты | Li3РО4 | Na3РО4 | K3РО4 | Rb3РО4 | Cs3РО4 |
| 9 | Сульфаты R2SО4 | Li2SО4 | Na2SО4 | K2SО4 | Rb2SО4 | Cs2SО4 |
| 10 | Хлориды RС1 | LiС1 | NaС1 | KС1 | RbС1 | CsС1 |
Элементы – образуют семейства со сходными свойствами:
Железа (d-элементы) платины (d-элементы)
Лантаноиды( f -элементы) Актиноиды ( f -элементы)
Ячейка (клетка)
| Порядковый (атомный) номер,  определяющий заряд ядра ( Z) - число протонов определяющий заряд ядра ( Z) - число протонов
12 Mg
Магний 24,305 Символ
Название элемента 
Аr 
о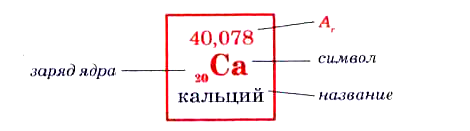 тносительная атомная масса элемента тносительная атомная масса элемента |
|
|
|
Заряд ядра равен атомному (порядковому) номеру элемента в системе.
| порядковый (атомный) номер элемента | заряд
= ядра= атома | число протонов в ядре | число =электронов в атоме | В ионе не равно ионе не равно в катионе в анионе ре р |
| запись элемента вне системы Менделеева | запись элемента в ячейке системы Менделеева |
| Полная запись количества элементарных частиц изотопа | Общепринятая запись изотопа |
|
| 
| А  Э Р
| 12 Mg
Магний 24.305 |
|  Массовое число А= р + n + е Массовое число А= р + n + е | Масса электрона не учитывается в массовом числе или Аr т.к. масса е в 2000 раз меньше массы р или n (масса электрона принимается за нуль) |
1913 Г Ван-ден-Брук присвоил элементам порядковый (атомный) номер,
а Мозли матиматически доказал физический смысл порядкового номера
тесты
| 75. Определите соответствие. галоген щелочной металл элемент II периода 
|
|
| Элементы X.Y.Z расположены в главных подгруппах, определить группу элемента .Z | элемент | Число валентных электронов | Число неспаренных электронов в основном состоянии | | X | а | b | | Y | а+1 | b+1 | | Z | а+2 | b |
| 6 группа 101 232 10 90 араз 2011 4гр |
| 66. Как называются элементы VIII группы главной подгруппы? А) щелочноземельные металлы В) галогены С) щелочные металлы D) халькогены Е) инертные газы |
|
|
|
|
|
|
|
|
|
|
| Определите порядковый номер элемента X, если относительная атомная масса его 23 и в ядре имеется 12 нейтронов. А) 40 В) 35 С) 23 D)11 E) 20 |
|










 естничная форма периодической системы элементов Д.И.Менделеева
естничная форма периодической системы элементов Д.И.Менделеева 
 1-3 малые периоды
1-3 малые периоды 


 классической форме – 8 групп
классической форме – 8 групп определяющий заряд ядра ( Z) - число протонов
определяющий заряд ядра ( Z) - число протонов 

 тносительная атомная масса элемента
тносительная атомная масса элемента  ионе не равно
ионе не равно


 Массовое число А= р + n + е
Массовое число А= р + n + е 










