Просмотр содержимого документа
«Табиғаттағы су айналымы»

Табиғаттағы су
Жұмахан А.Ж.

Оқу мақсаты
- 8.4.2.6.- судың табиғатта кең таралғандығын, қасиеттерін және тіршілік үшін маңызын түсіндіру.
- 8.4.2.7.- сулың табиғаттағы айналымын түсіндіру.

Судың табиғатта таралуы
Жер шарының 75%
Өсімдіктердің 90%
Тірі ағзада 60-70%
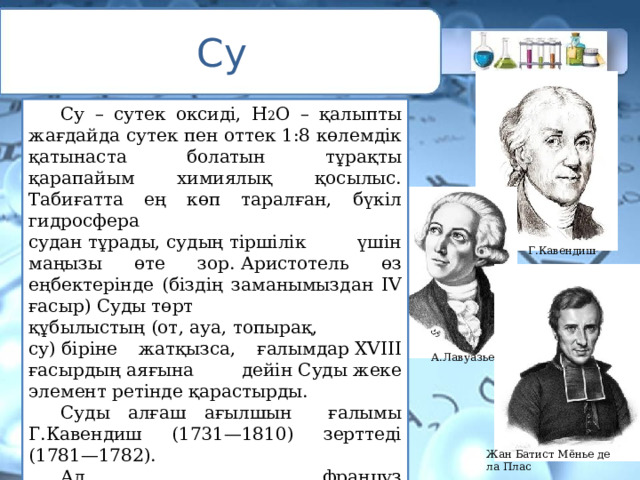
Су
Су – сутек оксиді, Н 2 О – қалыпты жағдайда сутек пен оттек 1:8 көлемдік қатынаста болатын тұрақты қарапайым химиялық қосылыс. Табиғатта ең көп таралған, бүкіл гидросфера судан тұрады, судың тіршілік үшін маңызы өте зор. Аристотель өз еңбектерінде (біздің заманымыздан IV ғасыр) Суды төрт құбылыстың (от, ауа, топырақ, су) біріне жатқызса, ғалымдар XVIII ғасырдың аяғына дейін Суды жеке элемент ретінде қарастырды.
Суды алғаш ағылшын ғалымы Г.Кавендиш (1731—1810) зерттеді (1781—1782).
Ал француз ғалымы А.Лавуазье (1743—1794) сутек жанғанда Су түзілетінін дәлелдеген (1783) және Ж.Меньемен бірге сандық құрамын анықтады (1785).
Г.Кавендиш
А.Лавуазье
Жан Батист Мёнье де ла Плас

Судың физикалық қасиеттері
Таза су – түссіз, иіссіз, дәмсіз сұйықтық. Судың қабаты 5 м асқанда көгілдір түсті болып көрінеді.
Қалыпты қысымда 100°С-та қайнайды да, 0°С-да мұзға (р=0,92 г/см 3 ) айналады, сондықтан мұз су бетінде қалқып жүреді. Сонда оның көлемі 9 %-ға артады. Судың беткі қабатының мұзбен қапталып жатуы ондағы тіршілік иелерінің қыс мезгілінде де өмір сүруіне жағдай жасайды.
Температурасы 4°С болғанда, тығыздығы 1г/см 3 (судың ерекшелігі). Судың жылу сыйымдылығы өте жоғары, оны мына мысалмен түсіндірейік. Жаздың аптап ыстық күндерінде су жылуды сіңіріп, өзеннің маңайын салқындатып тұрады, сондықтан адамдар оның жағалауына дем алуға көптеп барады.

Судың химиялық қасиеті
- Жай заттармен әрекеттесуі:
- I. Судың металдармен әрекеттесу реакцияларын сутегін ал әдістерінде қарастырған болатынбыз:
- 2Na + 2НОН = 2NaOH + Н 2 ↑
- Са + 2НОН = Са(ОН) 2 + Н 2 ↑
- Белсенділігі тым жоғары емес металл сумен әрекеттескенде оның оксиді түзіледі:
- Mg + НОН = MgO + H 2
- Белсенділігі төмен металдар сумен әрекеттеспейді.
- II. Бейметалдармен әрекеттесуі: Су кейбір бейметалдармен де әрекеттесе алады. Қыздырға көмірге су қоссақ екі түрлі газ қоспасы түзіледі — ол «су газы» деп аталады:
- С + НОН=СО↑+Н 2 ↑
- Көмірді жағарда оған су қосып шылайтынын білесіңдер, сонда түзілген екі газ да жанғыш екен. Хлорды суға жібергенде екі қышқылдың қоспасы түзіледі.
- Сl 2 + НОН = НСlO + HCl

Күрделі заттармен әрекеттесуі
- I. Активті металдардың оксидтерімен әрекеттесіп гидроксидтер (негіздер) түзеді.
- Na 2 О + Н 2 О = 2NaOH
- Әктасқа су қосқанда оның қайнай бастағанын көреміз, реакция жылу бөле жүреді:
- СаО + Н 2 О = Са(ОН) 2 + Q
- Металл оксидтері + су = негіз
- II. Кейбір бейметалдардың оксидтері сумен әрекеттескенде қышқыл түзеді. Күкірттің бір түйірін алып жақсак оның оксиді түзіледі:
- S + O 2 =SO 2
- Жану өнімін суға жіберсек:
- SО 2 + Н 2 О = H 2 SО 3
- күкіртті қышқыл түзіледі, көк лакмус қызарады. Дәл осындай реакциялар басқа бейметалдардың да оксидтерімен жүреді.
- Сl 2 О+ H 2 О = 2HClО
- N 2 O 3 + H 2 О = 2HNО 2
- Бейметалл оксидтері + су = қышқыл
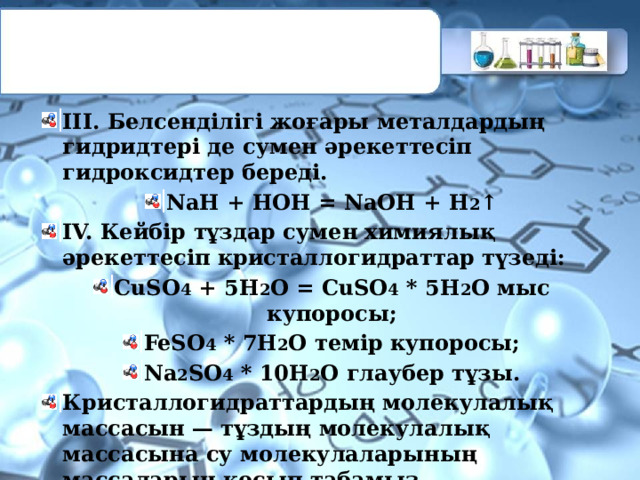
- III. Белсенділігі жоғары металдардың гидридтері де сумен әрекеттесіп гидроксидтер береді.
- NaH + НОН = NaOH + Н 2 ↑
- IV. Кейбір тұздар сумен химиялық әрекеттесіп кристаллогидраттар түзеді:
- CuSО 4 + 5H 2 О = CuSО 4 * 5H 2 О мыс купоросы;
- FeSО 4 * 7H 2 О темір купоросы;
- Na 2 SО 4 * 10H 2 О глаубер тұзы.
- Кристаллогидраттардың молекулалық массасын — тұздың молекулалық массасына су молекулаларының массаларын қосып табамыз.
- Mr(Na 2 CО 3 *10H 2 О) =106+180=286.
Су – еріткіш
Су — біршама инертті биологиялық еріткіш сүйықтық, онда кептеген органикалық жөне бейорганикалық заттар ериді, бірақ олардың ерігіштіктері әр түрлі. Қатты заттардың еруін біз қант пен тұзды еріткенде, ал газ күйіндегі заттардың еруін газдалған су ішкенде немесе суды қайнатқанда бөлінген көпіршіктерді байқау арқылы көрсек, сұйық күйіндегі заттардың еруін сірке суын еріткенде байқаймыз. Сонымен суда ерімейтін зат болмайды екен.
Ерігіштік — берілген температурада еріткіштің (су) 100 немесе 1000 грамында ери алатын зат массасымен және көлемімен анықталатын шама (г/100 г, г/1000 г Н 2 0, моль/л).
Ерігіштік заттың табиғатына тәуелді, мысалы: қант ерімтал болса, бор, әк нашар еритін заттар. Газ күйіндегі заттар үшін ерігіштік қысым мен температураға байланысты. Газдардың ерігіштігі қысым артқан сайын артады, ал температураны арттырғанда кемиді. Қатты заттардың көпшілігі үшін температураны арттырғанда ерігіштігі де артады.
Сұйық күйіндегі заттардың ерігіштігі олардың табиғатына байланысты, мысалы, спирт суда жақсы ерісе, ал бензин нашар ериді. табылады. Мысалы, Каспий теңізінде 13 г / л , Қара теңізде 19 г/л, Өлі Ерітінді деп еріткіш пен еріген заттан тұратын біртекті (гомогенді) жүйені айтады.
Берілген зат еріткіштің белгілі бір мөлшерінде осы температурада әлі де ери алатын болса, ерітінді қанықпаған, ал ери алмаса — қаныққан деп аталады.

Су айналымы
https ://youtu.be/j53Xfd2kPZQ

Бекіту тапсырмалары
- https://wordwall.net/ru/resource/57672616

- https://wordwall.net/ru/resource/57672927

Назарларыңызға рахмет!