| III. Оқушыларға сабақтың тақырыбын жариялау, оқыту мақсаттарымен және бағалау критерийлерімен таныстыру.
Оқушыларға металдар атомдары электрондарды беретін химиялық элементтер екенін, ал бейметалдар атомдары электрондарды қабылдайтын және беретін химиялық элементтер екенін естеріне салу керек.
Оқушыларға магний мен хлор атомдары арасында электрондарды беру және қабылдау процесін жазуды ұсыну. Олардан қосылыстарда химиялық байланыс қалай түзілетіндігін сұрау?
Қандай бөлшектер байланысты түзуге қатысады? Одан соң егер екі бейметалдың атомдары өзара әрекеттесе не болатындығын сұраңыз? Мысалы, күкірт пен оттегі атомдары арасында
Атомның өзіне басқа атомдардан валентті электрондар тарту қабілеті ретінде электртерістілік (ЭТ) ұғымын естеріне салыңыз. 1-қосымша Оқушыларға химиялық қосылыстарда қосылыстар түзілетін иондар зарядтары тотығу дәрежесі деп аталатындығын түсіндіру. Тотығу дәрежесі — бұл барлық қосылыстар (ионды, ковалентті-полярлық) тек иондардан құралады деген болжамның негізінде есептелген қосылыстағы химиялық элемент атомдарының шартты заряды.
Оқушыларға жұппен машықтану жаттығуларын орындауды ұсыну. 1-тапсырма. Мына элементтердің қосылыстары формулаларын құраңыз, олардың тотығу дәрежелерін атаңыз: а) магний мен күкірт; в) натрий мен фосфор; c) литий мен азот; d) хлор мен күкірт. Оқушылардың жұмыс нәтижелерін бағалаңыз. Оқушылармен «тотықтырғыш агент» және «тотықсыздандырғыш агент»терминдерін талқылаңыз. Ж азылған мысалдардан тотықтырғыш және тотықсыздандырғыш агенттерді, тотыққан және тотықсызданған агенттерді анықтауды ұсыныңыз. азылған мысалдардан тотықтырғыш және тотықсыздандырғыш агенттерді, тотыққан және тотықсызданған агенттерді анықтауды ұсыныңыз. Оқушыларға Mg + Cl2MgCl2реакциясының негізінде тотығу және тотықсыздандыру біруақытта өтетін процестер екендігін көрсету қажет.

Қабылданған электрондар саны = берілген электрондар саны. Қабылданған және берілген электрондардың санын көрсететін қосылыстағы заряд– бұл тотығу дәрежесінің мәні.  Мұғалімнің тотығу-тотықсыздану процесінің өзара байланыстылығын түсіндіруі. Тотығу және тотықсыздану – әрқашан біруақытта жүретін процестер. Бір зат тотыққанда, екіншісі тотықсызданады және керісінше болады. Тотығу және тотықсызданудың кез келген реакциясытотығу-тотықсызданудың бірыңғай процесін құрайды: Zn + Cl2 = ZnCl2. ZnмұндаZn2+дейін тотығады, ал Cl2болса 2Cl–дейін қалпына келеді. Мына ұғымдарды енгізу: тотықтандырғыш/тотықсыздандырғышнемесе тотықтандырғыш агент, тотықсыздандырғыш агент; тотыққан зат/тотықсыздандырылған зат. Реакция барысында берілген және қабылданған электрондар санын анықтау үшін машықтану жаттығуларын орындауды ұсыну. 2-тапсырма. Мына мысалдардан тотықсыздандырғышпен берілген және тотықтырғышпен қабылданған электрондардыңсанын анықтаңыз:
а) Fe + HCl; c) Al + Fe2O3; в) Zn + Br2;d) Fe2O3 + C. Оқушыларға қосылыстарда тотығу дәрежесін анықтау үшін кейбір қағидаларды қолдану қажеттігін түсіндіру керек. 2-қосымша Оқушыларға өзгермейтін тотығу дәрежесі бар элементтерден басталатын тотығу дәрежелерінің кестесін көрсету. 3-қосымша Жұппен машықтану жаттығуларын орындауды ұйымдастыру. 3-тапсырма. Мына қосылыстарда тотығу дәрежесін анықтаңыз: MgO, ZnCl3, О2, Fe2O3, CaS, Na3N, P2O5, SiH4, NaH, AsH3, HNO3, CaSO4. Озат оқушылар үшін мына мысалдарды ұсынуға болады: Ca(OH)2, Ca3(PO4)2, (NH4)2CO3 жәнеCO32-, PO43-, OH-, MnO4-, Cr2O72- .
IV.Оқушыларға элементтердің тотығу дәрежесі қосылыстардың формулаларын дұрыс жазу үшін қолданылатындығын түсіндіріңіз. Тотығу дәрежесін, марганец оксидтерін (IV) және (II), көміртегі оксидтерін (IV) және (II), темір (III) және (II), күкірт (IV) және (VI) оксидтерін қолдана отырып, азот оксидтерінің атауын қайталаңыз. V.Айнымалы тотығу дәрежесі ұғымын енгізіңіз. Көптеген элементтерге айнымалы тотығу дәрежесі тән екендігін түсіндіріңіз. 
Тотығудың 3 дәрежесіндегімыс: A – металл мысы, 0 B – мыс хлориді (+1), C – мыс хлориді(+2) Одан әрі өзара тексере отырып, жұппен жұмысты ұйымдастырыңыз 4-тапсырма. Мына қосылыстардатотығу дәрежесін анықтаңыз: А) СО2, СН4, СО В) CrO, Cr2O3, CrO3, H2Cr2O7 С) AlCl3, Cl2O7, HClO, HClO3, HClO4 Тапсырма жаппай орындалады, алдымен оқушылар оны жұппен орындайды, одан соң кездейсоқ таңдау әдісімен (мұғалім оқушылардың аты жазылған жолақтарды алады), тақтада тапсырманы жазу үшін 4 оқушыны шақырамыз.Оқушылар жұмыстарды өзара бағалайды, дұрыс шешімін ұсынады, осыдан кейін өздерінің қателіктерін көрсетеді. Өзара бағалау және өзін-өзі бағалау ұсынылған табысқа жету критерийлеріне сәйкес өткізіледі. | 





 азылған мысалдардан тотықтырғыш және тотықсыздандырғыш агенттерді, тотыққан және тотықсызданған агенттерді анықтауды ұсыныңыз.
азылған мысалдардан тотықтырғыш және тотықсыздандырғыш агенттерді, тотыққан және тотықсызданған агенттерді анықтауды ұсыныңыз. 




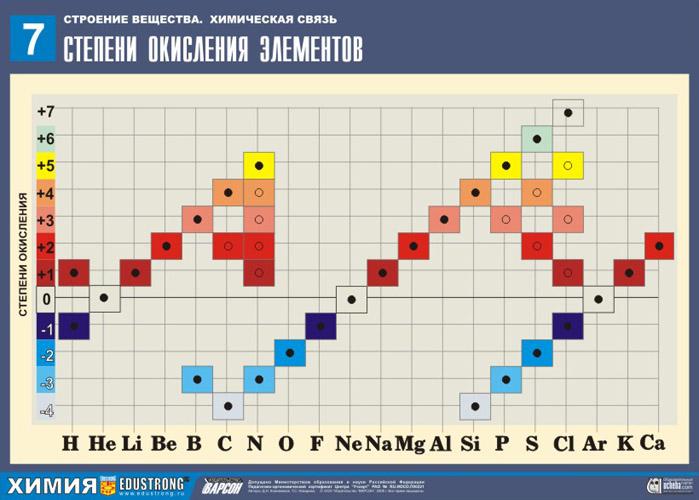

 -қосымшаТотығу дәрежесін анықтау ресурсы
-қосымшаТотығу дәрежесін анықтау ресурсы











