

СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой
Организационный момент
Проверка знаний
Объяснение материала
Закрепление изученного
Итоги урока


Исследовательская работа " Состав почвы"
Просмотр содержимого документа
«Исследовательская работа " Состав почвы"»
Содержание
Введение..............................................................................................................................................3
1. Обзор литературы
1.1. Общая характеристика гуминовых веществ
1.1. Общая характеристика строения и свойств гуминовых веществ ......................................4
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ........................................................................................29
2.1. Реактивы и оборудование....................................................................................................29
2.2. Техника эксперимента .........................................................................................................30
2.2.1. Выделение гуминовых кислот........................................................................30
2.2.4. Методики исследования состава, строения и свойств гуминовых кислот .....................33
3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ...................................................................................38
Выводы..............................................................................................................................................67
Список литературы...........................................................................................................................68
Введение
Тема данной курсовой работы находится в предметной области сразу нескольких наук. Изучением гуминовых веществ занимается органическая химия, химия почв, биогеохимия, почвоведение, агрономия, экология и охрана биосферы, теория минерального питания растений.
История открытия гуминовых веществ берет свое начало в XVIII веке. Первые результаты исследований в данной области связаны с работой Ф.Ахарда, который действием раствора щелочи на почву и на торф получил темно-бурый раствор. Десятью годами позже Л.Вокелен выделил аналогичное вещество из ствола старого вяза. Т.Томсон в 1807 г. назвал это вещество ульмином (от ulmus - вяз). Много внимания гуминовым веществам уделил великий шведский химик Я. Берцелиус.
В последние полвека значительный вклад в изучение гуминовых веществ внесли русские и советские ученые, преимущественно почвоведы: И.В. Тюрин, М.М. Кононова, С.С. Драгунов, Л.Н. Александрова, многие исследователи зарубежных стран, в их числе В. Фляйг (ФРГ), Ф. Дюшофур (Франция), Т. Хаяси (Япония), М. Шнитцер (Канада), Ф. Стевенсон (США), М.Х.Б. Хейес (Англия) и др. В 1981 году было принято решение о создании Международного общества по изучению гуминовых веществ (International Humic Substances Society - IHSS).
К настоящему времени разработаны методы выделения ГВ из различных природных объектов, определены их химический состав, все важнейшие свойства, изучено влияние на почвы, растения, микроорганизмы, рыб, животных. Выявлены возможности использования ГВ в промышленном производстве и сельском хозяйстве. Первые работы по гуминовым удобрениям принадлежат Л.А. Христевой, С.С. Драгунову и другим ученым.
Гуминовые вещества представляют собой обширный и реакционноспособный класс природных соединений, входящих в состав органического вещества почв, природных вод и твердых горючих ископаемых. Наличие в молекулах ГВ широкого спектра функциональных групп, таких как карбоксильные, гидроксильные и другие в сочетании с присутствием ароматических фрагментов обуславливает их способность вступать во взаимодействия с различными типами экотоксикантов, такими как металлы, радионуклиды и органические соединения, тем самым снижая их токсическое воздействие на живые организмы и экосистемы.
Гуминовые вещества находятся в составе гумуса. Это более или менее темноокрашенные, азотосодержащие высокомолекулярные соединения, образующиеся в почвах, торфах, углях, других природных телах. Они накапливают элементы питания и энергию, участвуют в миграции катионов, снижают негативное действие токсичных веществ, влияют на развитие организмов и тепловой баланс планеты. Они устойчивы, высокомолекулярны, полидисперсны, содержат различные функциональные группы, аминокислоты, полисахариды, бензоидные фрагменты.
Содержательная часть данной работы построена главным образом на анализе литературных источников и научных результатов, полученных различными ученым.
Целевая установка курсовой работы состоит в раскрытии природного происхождения, биологических функций и химического состава гуминовых веществ.
Обзор литературы
Качественная характеристика и классификация торфа
Торф – ценнейший природный биологический материал. Из всех видов твердых видов топлива – это самое молодое отложение, образующееся естественным образом, путем разложения отмерших частей деревьев, кустарников, трав и мхов, в условиях повышенной влажности и ограниченного доступа кислорода. От почвенных образований торф принято отличать по содержанию в нём органических соединений – не менее 50% по отношению к абсолютно сухой массе.
Органическое вещество торфа состоит из растительных остатков, претерпевших различную степень разложения. Перегной (гумус) придает торфу тёмную окраску. Относительное содержание в общей массе торфа продуктов распада растительных тканей, утративших клеточную структуру, называют степень разложения торфа.
Различают торф слаборазложившийся (до 20%), среднеразложившийся (20-35%) и сильноразложившийся. Торф имеет сложный химический состав, который определяется условиями генезиса, химическим составом растений-торфообразователей и степенью разложения.
В соответствии с составом исходного растительного материала, условиями образования торфа и его физико-химическими свойствами торф относят к одному из 3 типов: верховому, переходному и низинному.
Принцип образования торфяной залежи представлен на рис. 1.
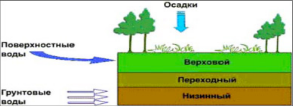
Рис. 1. Принцип образования торфяной залежи
Каждый тип по содержанию в торфе древесных остатков подразделяется на три подтипа: лесной, лесотопяной и топяной. Торф разных подтипов отличается по степени разложения. Торф лесного подтипа имеет высокую степень разложения, иногда до 80%.
У топяного торфа – минимальная степень разложения. Лесотопяной занимает промежуточное положение.
Общетехнические и агрохимические свойства торфа
Растительный покров торфяного месторождения, являясь чувствительным реагентом на изменение водно-минерального питания, находит отражение в ботаническом составе торфа и поэтому дает представление о его минеральной и органических частях.
При выборе направления использования торфа в сельском хозяйстве большое значение придается его видовой принадлежности. Например, установлено, что торф травяной и древесной групп богаче гуминовыми веществами и азотом, чем моховой, но беднее углеводами. Древесные виды торфа содержат еще больше гуминовых веществ и меньше углеводов по сравнению с травяными.
По ботаническому составу можно судить о водопоглотительных свойствах торфа, которые значительно выше у видов торфа моховой и травяно-моховой групп, чем у древесной и древесно-травяной.
Важной характеристикой торфа является его показатель степени разложения. Она колеблется в широком диапазоне – от 1-5 до 60-80%. С ее возрастанием количество углеводов в торфе уменьшается, а гуминовых веществ увеличивается.
Степень разложения при определенном ботаническом составе оказывается большое влияние на влагоемкость торфа – по мере ее снижения влагоемкость возрастает.
Со степенью разложения в той или иной мере связаны почти все другие свойства торфа. С геоботаническим составом и степенью разложения наиболее тесно связаны свойства и показатели торфа верхового типа. У торфа низинного типа с повышением содержания зольной части и такая связь почти не выявляется.
Сельскохозяйственная ценность торфа во многом, а иногда и в основном определяется его органической частью. Органическое вещество торфа состоит из битумов, гуминовых веществ, угдеводов, трудногидролизуемых веществ (или целлюлозы) и негидролизуемого остатка (лигнина).
Гуминовая часть представляет для земледелия наибольшую ценность. В составе гуминовых веществ различают гуминовые кислоты и фульвокислоты. Несмотря на большое количество исследований, структура гуминовой кислоты и природа ее образования еще далеко не изучены. Установлено, что природные гуминовые вещества почвы из торфов представляют собой соединения кислотной природы, содержащие ароматические комплексы и белковоподобные компоненты, отщепляющие при гидролизе аминокислоты. Всего обнаружено более 17 аминокислот. В наибольшем количестве встречаются глютаминовая кислота, глицин и треонин.
Гуминовые кислоты, имея различный химический состав, но общий тип строения, относятся к гетерополиконденсатам, не являющимися химически индивидуальными соединениями.
Состав и содержание гуминовых веществ различны не только в пределах групп торфов, но и для одного и того же вида. Среднее содержание гуминовых кислот в торфе низинного типа составляет 38-40 %, переходного – 35-39 %, верхового – 24-26 %, фульвокислот – 16-17 % для торфа низинного типа, 17-19 % для переходного и верхового.
Гуминовые вещества представлены гумусовыми кислотами, прогуминовыми веществами и гумином.
Гумусовые кислоты представляют собой азотосодержащие высокомолекулярные оксикарбоновые кислоты с интенсивной темно-бурой окраской1.
Гумусовые кислоты по растворимости разделяют на гуминовые кислоты, гиматомелановые кислоты и фульвокислоты.
В состав гумуса входят гуминовые кислоты, фульвокислоты и гумины.
Гуминовые кислоты — это группа веществ темного цвета, которые выделяются из почвы щелочами и осаждаются кислотами. Они характеризуются высоким содержанием углерода (50—62 %), аморфным состоянием, полидисперсностью (различной величиной частиц) и гетерогенностью.
При взаимодействии с катионами гуминовые кислоты образуют соли — гуматы. Гуматы одновалентных катионов К+, Na+, N+ образуют в почве коллоидные растворы — золи, которые легко растворяются и вымываются из почвы. Гуматы двух- и трехвалентных катионов (Са2+, Mg2+, Al3+, Fe3+) находятся в почве в виде нерастворимых гелей, не вымываются, накапливаются в местах образования, больше всего их в верхних слоях почвы.
Гуминовые кислоты — наиболее ценная часть гумуса, они имеют большую собирательную поверхность, играют важную роль в образовании агрономически ценной структуры почвы и основного фонда питательных веществ (прежде всего азот для растений).
Фульвокислоты — это гуминовые вещества желтого или красного цвета, которые остаются в растворе после выпадения в осадок гуминовых кислот. Фульвокислоты отличаются от гуминовых меньшим содержанием азота, более высокой кислотностью, высокой растворимостью в воде их соединений с минеральной частью почвы. Благодаря высокой кислотности фульвокислоты разрушают почвенные минералы и способствуют перемещению продуктов разложения в нижние слои почвы.
Гумины представляют собой комплекс гуминовых веществ с меньшим содержанием углерода и состоят из тех же гуминовых и фульвокислот, высоко полимеризованных, уплотненных и более тесно связанных между собой.
извлечения щелочью, а поэтому состав гуминов зависит от процедуры извлечения, согласно второму направлению, в состав гуминов входят отмершие остатки растений, следовательно, их состав зависит от биохимического состава отмерших остатков.
Прогуминовые вещества (или меланины) представляют собой высокомолекулярные темноокрашенные биогенного происхождения пигменты, образующиеся при окислительной полимеризации фенольных соединений, включая и азотсодержащие (Александрова, 1980).
Гуминовые кислоты — группа гумусовых кислот, растворимая в щелочах и нерастворимая в кислотах. Их соли носят название гуматы. ГК слабо растворимы в воде, с одновалентными катионами (К+, Na+, NH4+) образуют водо-растворимые соли, а с двух-и трехвалентными катионами (Са2+, Mg2+, Al3+, Fe3+) легко выпадают в осадок (Кононова, 1951; 1963;
11 Орлов, 1974; 1990; Александрова, 1980; Пономарева, Плотникова, 1980; и
ДР-).
Группа гуминовых кислот разделяется на две подгруппы: чёрные (серые)
и бурые гуминовые кислоты. Разделение чёрных и бурых гуминовых кислот может быть осуществлено методом высаливания: в 2 н. растворе NaCl чёрные гуминовые кислоты коагулируют и выпадают в осадок. (Орлов, 1985). Эти две подгруппы отличаются по содержанию углерода, оптической плотности и другим признакам. Так, у бурых гуминовых кислот оптическая плотность в 2 раза ниже, чем у черных гуминовых кислот, больше относительная молекулярная масса, они более гетерогенны, имеют рыхлую химическую структуру и более лиофильны (Орлов, 1974). Черные гуминовые кислоты характеризуются сродством к Са2+, в то время как бурые гуминовые кислоты — к полуторным оксидам (Пономарева, Плотникова, 1980).
Основным подходом к решению задач разделения гумусовых кислот на группы является использование прямого межфазного массообмена в тех вариантах растворения-осаждения, которые базируются на распределении макромолекул между раствором и осадком (гелем) в зависимости от их размера и состава. Эти варианты обычно включают разделение щелочного раствора ГВ на сложную смесь веществ, одни из которых, выделяющиеся из фазы раствора при его подкислении, — гуминовые кислоты, а компоненты, остающиеся в надосадочной жидкости, — фульвокислоты. Компоненты, переходящие в раствор при обработке свежего осадка гуминовых кислот этанолом (реже ацетоном или диоксаном), определяют как гиматомелановые кислоты. Результаты разделения ГВ в значительной степени зависят от условий проведения эксперимента. Способы расчета равновесия между раствором и гелем для ГВ не разработаны, и процесс разделения описывается на феноменологическом уровне [Шинкарёв и др., 2000].
До сих пор главный принцип разделения гумусовых веществ на гуминовые кислоты и фульвокислоты основан на предположении, что гуминовые кислоты нерастворимы в сильно кислых растворах при рН~ 1-2 (Кононова, 1963; Комиссаров, 1978; Александрова, 1980; Пономарева, Плотникова, 1980; Senesi et al., 1983; Орлов, 1990; Swift, 1996; и др.). Существует мнение (Попов, Бурак, 1998; Popov, 1998), что разделение гумусовых соединений на гуминовые кислоты и фульвокислоты обусловлено различной агрегативной устойчивостью этих групп специфических соединений. Агрегативную устойчивость (устойчивость к агрегации) дисперсной системы определяют по скорости коагуляции, она носит термодинамический характер. В такой дисперсной системе поверхностная энергия скомпенсирована энтропийной составляющей, благодаря чему система проявляет термодинамическую агрегативную устойчивость и в ней не происходит процесс коагуляции (Фролов, 1988). В связи с этим потеря агрегативной устойчивости частиц дисперсной фазы ГВ (в частности молекул гуминовых кислот) приводит к их коагуляции и, как следствие, осаждению в сильно кислой среде (при рН~1-2). Таким образом, из находящихся в растворе ГВ, лишь ГК могут представлять собой агрегативно неустойчивую систему (Попов, Бурак, 1998; Popov, 1988).
Разделение смеси гумусовых кислот на ГК и ФК также связано с гидрофильно-гидрофобным балансом амфифильных молекул ГВ. Известно (Фролов, 1988), что гидрофильность карбоксильной группы (-СООН), замещенной ионом водорода ниже, чем содержащей катионы Na+ или К+ (-COONa и -COOK). При подкислении (до рН~1-2) достаточно концентрированного щелочного раствора гумусовых кислот (Сорг. ^0,1 мг/мл) происходит замещение ионов натрия и калия на ион водорода в кислых функциональных группах, вследствие этого гидрофильно-гидрофобный баланс ГК ещё больше сдвигается в гидрофобную сторону. В результате ГК теряют свою агрегативную устойчивость и выпадают в осадок. Выявлено (Попов, Бурак, 1998), что при содержании гумусовых кислот в количестве, не превышающем определённую концентрацию (например, при
13
Сорг.
1.1. Общая характеристика строения и свойств гуминовых веществ
Гуминовые вещества (ГВ) это – более или менее темноокрашенные, азотосодержащие высокомолекулярные соединения. Они накапливают элементы питания и энергию, участвуют в миграции катионов, снижают негативное действие токсичных веществ, влияют на развитие организмов и тепловой баланс планеты. Они устойчивы, высокомолекулярны, полидисперсны, содержат различные функциональные группы, аминокислоты, полисахариды, бензоидные фрагменты.
ГВ - это сложные смеси устойчивых к биодеструкции высокомолекулярных темно-окрашенных органических соединений природного происхождения, образующихся при разложении растительных и животных остатков под действием микроорганизмов и абиотических факторов среды. ГВ составляют от 60 до 80% органического вещества водных и почвенных сред [1-6].
ГВ представлены гумусовыми кислотами, прогуминовыми веществами и гумином.
Гумусовые кислоты представляют собой азотосодержащие высокомолекулярные оксикарбоновые кислоты с интенсивной темно-бурой окраской.
Гумусовые кислоты по растворимости разделяют на гуминовые кислоты, гиматомелановые кислоты и фульвокислоты.[1]
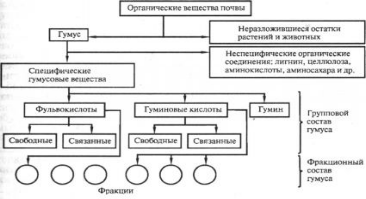
Рис.1 (http://www.zoodrug.ru/topic3547.html)
В основе процесса химического и биологического разложения растений и животных остатков лежит отбор устойчивых к биодеградации структур и соединение их в макромолекулы. В отличие от синтеза биополимеров, протекающего по заданному генетическому коду, процесс образования ГВ подчиняется статистическим принципам [7-9]. По этой причине ГВ представляют собой смесь макромолекул переменного состава и нерегулярного строения [10, 11].
Общепринятая классификация ГВ [9, 10, 12] основана на различии в их растворимости в кислотах и щелочах. Согласно этой классификации ГВ подразделяют на три основные составляющие: гумин – неизвлекаемый остаток, нерастворимый ни в щелочах, ни в кислотах; гуминовые кислоты (ГК) – фракция ГВ, растворимая в щелочах и нерастворимая в кислотах; фульвокислоты (ФК) – фракция ГВ, растворимая в щелочах и кислотах.
Макромолекулы гуминовых веществ состоят из «каркасной» (негидролизуемой) и периферической (гидролизуемой) части [2, 3, 10, 11]. Каркасная часть представлена высокозамещенными ароматическими фрагментами, соединенными алкильными, эфирными и др. мостиками. Преобладающими заместителями являются кислородсодержащие функциональные группы: карбоксильные, фенольные и спиртовые гидроксильные, карбонильные и метоксильные [2,9,13,14]. Периферийная часть представлена углеводно-протеиновым комплексом, ковалентно связанным с каркасной частью. Так, по данным [15] до 30% от массы ГВ представляют собой углеводные фрагменты. Кроме того, в периферийную часть входят зольные компоненты – силикаты, алюмосиликаты, оксиды железа и т.п., связанные с органической матрицей кислородными мостиками [2, 16]
Для более наглядной характеристики структуры ГВ часто прибегают к следующему приему: объединяя структурные фрагменты ГВ между собой, умозрительно связывают их в среднюю молекулу, свойства которой определяются соотношением структурных фрагментов [17]. Существует целый ряд структурных формул средних молекул ГВ, при построении которых авторы прибегали к различным процедурам [2]. На рис.1.1 приведена одна из них, которая, наиболее наглядно демонстрирует стохастический характер структуры ГВ [18].
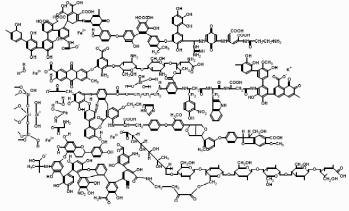
Рис. 1.1. Гипотетическая структура гуминовых веществ почвы
Представление структуры ГВ средней молекулой является наиболее близким к классическому описанию органических веществ посредством структурных формул. Оно позволяет продемонстрировать основные химические свойства ГВ, такие как кислотность, хелатирующая способность, окислительно-восстановительные и π-акцепторые свойства, а также полиэлектролитную природу ГВ. Однако такое представление не лишено недостатков. Во-первых, оно сводит все многообразие молекулярных структур ГВ к единственной - средней. Во-вторых, корректность формулы во многом зависит от принципа объединения структурных фрагментов, которых придерживался ее автор. Например, недостатком структуры, приведенной на рис. 1.1, является завышенное количество азотсодержащих функциональных групп.
Структура ГВ обусловливает их способность к широкому спектру химических взаимодействий, что определяет многообразие их функций в окружающей среде. Так, ГВ выполняют функции депо питательных веществ и микроэлементов, способствуют их транспорту в растения, участвуют в структурировании почвы [2], повышают ее катионо-обменную и буферную емкость. Кроме того, в настоящее время все большее значение приобретает защитная функция ГВ, а именно, их способность взаимодействовать с различными типами загрязняющих веществ, снижая их подвижность и токсичность для живых организмов [7-11].
СХЕМЫ СТРОЕНИЯ МОЛЕКУЛ ГВ.
Точных молекулярных формул для любых ГВ не существует, все предложенные варианты имеют характер схем, они гипотетичны, поскольку учитывают только состав соединений и некоторые их свойства, тогда как расположение атомов и атомных групп остается при этом неизвестным. Несмотря на это, попыток составления молекулярных формул ГВ в истории науки было немало: сейчас насчитывается не один десяток таких формул, часть которых имеет только характер блок-схем, а часть отражает более или менее реально состав и свойства гуминовых кислот. В качестве примера можно привести блок-схему, которую предложили польские ученые В. Мистерски и В. Логинов в 1959 году, и гипотетическую схему строения, отражающую все известные сегодня данные о составе и свойствах гуминовых кислот (рис. 5).
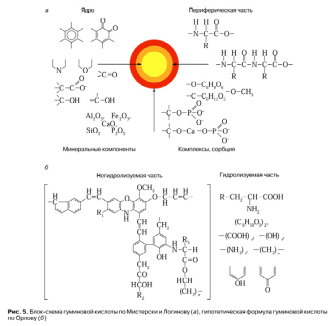
Негативные результаты при попытках составления структурных формул ГВ объясняются тем, что последние не образуют кристаллов, имеют переменный состав и полидисперсны даже в наиболее однородных препаратах. Получить мономолекулярные фракции ГВ пока не удалось. Поэтому к ним оказались неприменимыми те методы и приемы, которые обычно используют для создания формул природных и высокомолекулярных биоорганических молекул.
1.1.1. Элементный состав гуминовых веществ
Хорошо изучено содержание различных химических элементов в этих веществах. Содержание углерода в массовых долях колеблется от 40 до 60 % в зависимости от происхождения и источника ГВ. Азот есть всегда, это доказал еще русский ученый Р. Германн в середине прошлого века, но его мало — 3—5 %. Водорода обычно содержится 3—6 %, а кислорода — 33—37%. Обязательно входят сера — до 0,7—1,2 % и фосфор — до 0,5 %.], обязательной составной частью являются микроэлементы [19] и вода [2]. Всегда есть разные металлы, хотя пока трудно сказать, обязательны ли они для ГВ или просто являются примесью, поскольку очистить ГВ нелегко. Например, в препаратах ГВ были найдены мелкокристаллический кварц Si02, мелкокристаллический гетит FeOOH, что приходится признать явными примесями.[4/]
Брутто-формулу ГВ можно записать в общем виде следующим образом:
CxHyNzOpSqMr (Al2O3)l (SiO2)m (H2O)n,
где: М – ионы металлов, x, y, z, p, q, l, m, n – стехиометрические коэффициенты.
Средний элементный состав органической части ГВ различного происхождения приведен в табл. 1.1, являющейся результатом статистической обработки данных по элементному составу препаратов ГВ [20].
Таблица 1.1
Средний элементный состав гуминовых веществ различного происхождения
(в расчете на беззольную навеску, n – число препаратов, ± стандартное отклонение)
| Препарат | Содержание элементов, масс. % | Атомные отношения | ||||||
| С | Н | О(1) | N | S | О/С | Н/С | ||
| ГК почв (n=215) ФК почв (n=127) ГК торфа (n=23) ФК торфа (n=12) ГК вод (n=56) ФК вод (n=63) ГК морских д.о.(2) (n=95) ФК морских д.о. (n=12) | 55.4±3.8
45.3±5.4
57.1±2.5
54.2±4.3
51.2±3 46.7±4.3 56.3±6.6
45.0±4.0 | 4.8±1.0
5.0±1.0
5.0±0.8
5.3±1.1
4.7±0.6 4.2±0.7 5.8±1.4
5.9±0.9 | 36.0±3.7
46.2±5.2
35.2±2.7
37.8±3.7
40.4±3.8 45.9±5.1 31.7±7.8
45.1±6.0 | 3.6±1.3
2.6±1.3
2.8±1.0 (n=21) 2.0±0.5
2.6±1.6 2.3±1.07 3.8±1.5
4.1±2.3 | 0.8±0.1 (n=67) 1.3±0.5 (n=45) 0.4±0.2 (n=12) 0.8±0.2 (n=11) 1.1±0.3 (n=13) 1.2±0.7 (n=14) 3.1±1.4 (n=66) 0.8±0.6 (n=11) | 0.50±0.09
0.78±0.16
0.47±0.06
0.53±0.09
0.6±0.08 0.75±0.14 0.45±0.18
0.77±0.17 | 1.04±0.25
1.35±0.34
1.04±0.17
1.20±0.33
1.12±0.17 1.10±0.13 1.23±0.23
1.56±0.13 | |
Примечание: подавляющее большинство данных по содержанию кислорода получено по разности; д.о. – донные отложении.
Как видно из табл. 1.1, содержание углерода в ГВ различного происхождения варьируется от 50 до 60 %, кислорода – от 30 до 40 %.
Атомные соотношения H/C и О/С позволяют оценить такие параметры структуры, как содержание ненасыщенных фрагментов и кислородсодержащих функциональных групп. Так, при соотношении Н/С пресные воды торфа ≈ почвы.
ФК характеризуются более низким содержанием углерода и более высоким – кислорода.
Это предполагает большую степень замещения ароматического каркаса ФК кислородсодержащими функциональными группами. Максимальное содержание кислорода характерно для ФК пресных вод.
Как показано в работах [21, 22] различия в структурах и элементном составе ГВ разных природных сред непосредственно связаны с источниками гумусообразования в этих системах. Так, в торфах, почвах и пресных водах основными предшественниками ГВ являются продукты разложения лигнина, полифенолы и производные фенолов, синтезируемые микроорганизмами, то есть вещества, обогащенные ароматическими структурами [23]. ГВ морских вод и донных отложений образуются, преимущественно, из остатков водорослей и планктона, главными компонентами которых являются липиды, полисахариды и пигменты- соединения алифатического и алициклического характера [16, 24].
Известно также, что элементный состав ГВ одинакового происхождения может варьировать в зависимости от конкретного источника: различного типа почв [20], вод [4] и т.д.
Таким образом, определение элементного состава является одним из ключевых этапов при анализе структуры ГВ [25, 26].
1.1.2. Функционально-групповой состав гуминовых веществ
Наличие большого количества функциональных групп в составе как ароматического каркаса, так и алифатической периферии, обеспечивает высокую комплексообразующую способность ГВ и их способность участвовать в окислительно-восстановительных реакциях. Благодаря этому ГВ оказывают значительное влияние на поведение тяжелых металлов и органических загрязняющих веществ в почвенных и водных системах.
В настоящее время в гуминовых веществах обнаружено более десяти различных типов функциональных групп: карбоксильные, фенольные и спиртовые гидроксильные, карбонильные, хинонные, метоксильные, сложноэфирные, енольные, амино-, амидо- и имидогруппы, сульфо-, тиольные и дисульфидные группы [9]. Поскольку суммарное содержание серы и азота в ГВ обычно не превышает 5%, можно считать, что химическое поведение гуминовых веществ определяется, в основном, кислородсодержащими функциональными группами.
Согласно литературным данным [12, 27, 28], содержание функциональных групп в ГВ варьируется в зависимости от источника происхождения. Препараты водного происхождения, как правило, характеризуются повышенным содержанием карбоксильных групп [29]. Однако более отчетливо прослеживается уже отмеченная тенденция: независимо от источника происхождения, ФК характеризуются более высоким содержанием карбоксильных групп, чем ГК.
Кислородсодержащие группы. Кислород входит как в каркасную, так и периферийную части молекулярного ансамбля ГВ, составляя от 20 до 35 % масс. В ароматической части он находится преимущественно в составе карбоксильных и гидроксильных групп, в периферийной части – в углеводных фрагментах [30]. Обобщенные сведения о распределении кислорода по различным функциональным группам в ГВ приведены в табл. 1.2.
Таблица 1.2
Распределение кислорода между функциональными группами в ГВ почв
| Общее содержание кислорода, % | Функциональные группы | Учтенный кислород, % | |||
| СООН | СArOH | СAlkOH | C=O | ||
| % кислорода | |||||
| Почвенные гуминовые кислоты | |||||
| 37.2 36.8 35.4 | 24 26 18 | 33 25 38 | 10 15 13 | 8 7 4 | 75 74 73 |
| Почвенные фульвокислоты | |||||
| 47.3 44.8 47.7 | 58 65 61 | 19 12 9 | 12 13 16 | 6 9 4 | 95 99 90 |
Как видно из табл. 1.2, около 75% кислорода в ГК и около 95% – в ФК распределено между четырьмя основными типами функциональных групп: карбоксильными, фенольными и спиртовыми гидроксильными, и карбонильными, причем вклад этих групп в общее содержание кислорода различен для ГК и ФК. Вышеперечисленные функциональные группы (в первую очередь, карбоксильные и фенольные), вносят определяющий вклад в комплексообразующую способность гуминовых веществ по отношению к тяжелым металлам.
Азотсодержащие группы. Содержание азота в ГВ составляет 1-5% (табл. 1.1). Часть азота (40-60%) входит в состав каркасной части [10, 31]. Остальной азот находится в составе периферической части. По данным, опубликованном в обзоре [32], азот периферической части распределяется следующим образом: 20-45% входит в состав аминокислотных остатков, 2-8% – в состав аминосахаров, 8-15% присутствует в виде солей аммония, до 20% – в виде неустановленных фрагментов. При этом азот каркасной части ГВ находится в составе следующих групп: NH2- группы, связанные с ароматическими кольцами; -NH- и =N- группы в открытых цепях; индольные, пиррольные и пиридиновые кольца; мостиковые NR-группы, связывающие хинонные кольца; аминокислоты, связанные с ароматическими ядрами через атом азота.
Из приведенных фрагментов алифатические амины, аминокислоты и гетероциклы способны образовывать комплексные соединения с металлами. Таким образом, указанные группы, наряду с кислородсодержащими, могут влиять на реакционную способность ГВ по отношению к металлам.
Серосодержащие группы. Согласно публикации [22], распределение серы в торфяных гуминовых веществах можно представить следующим образом (в % от общей серы): 8-12% – лабильные сульфонатные группы, 3-6% – аминокислоты, 4-19% – эфиры серной кислоты, 54-70% – тиолы, S-гетероциклы, стабильные сульфонаты, 3-23% – алифатические сульфиды.
Хинонные и семихинонные фрагменты. Методом ЭПР показано, что содержание неспаренных электронов в ГВ составляет (0.1-40)·1016 спин/г [33]. Присутствие данных групп обусловливает возможность протекания реакций с участием ГВ по свободнорадикальному механизму, в частности, восстановление ионов металлов и декарбоксилирование отдельных фрагментов ГВ. Окислительно-восстановительные переходы хинонных, семихинонных и гидрохинонных фрагментов определяют окислительно-восстановительные свойства гуминовых веществ [34].
Таким образом, наличие большого числа функциональных групп, таких как – NH2, -OH, -COOH, -CONH2, -SH позволяет рассматривать ГВ как высокореакционные вещества, способные реагировать с широким классом химических соединений. С другой стороны, это открывает большие возможности для химической модификации гуминовых веществ.
1.1.3. Характеристика структуры гуминовых веществ
ГВ являются природными полимерами переменного состава и нерегулярной структуры [2]. Для описания характеристик такого объекта, используется предположение, что вещество нерегулярного строения состоит из ограниченного числа более мелких фрагментов. Это позволяет охарактеризовать структуру объекта через его фрагментный состав.
Одним из основных методов исследования структуры органических соединений является спектроскопия ЯМР.
Типичный 13С ЯМР спектр гуминовых веществ приведен на рис 1.2, из которого видно, что полидисперсность и химическая гетерогенность ГВ приводит к тому, что их 13C ЯМР спектры не содержат разрешенных индивидуальных пиков, представляя собой суперпозицию большого числа сигналов.
Общим подходом к интерпретации получаемых 13С ЯМР спектров немодифицированных ГВ является разбиение на спектральные диапазоны, соответствующие сигналам атомов углерода со сходным химическим окружением (табл. 1.3).
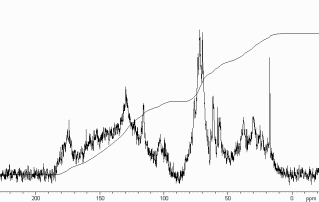
Рис. 1.2. Типичный 13С ЯМР спектр ГВ почв
Таблица 1.3
Основные диапазоны сигналов в 13С ЯМР спектре гуминовых веществ
| Диапазон химических сдвигов | Типы атомов углерода |
| 5-48 м.д. | алифатические С- и H-замещенные атомы углерода (CAlk); |
| 48-90 м.д. | алифатические атомы углерода, связанные простой связью с гетероатомом (кислородом илиазотом), в основном карбогидратного типа (CAlk-O) |
| 90-108 м.д. | ацетальные атомы углерода, связанные простыми связями с двумя атомами кислорода (CO-Alk-O) |
| 108-145 м.д. | ароматические С- и Н-замещенные атомы углерода (CAr-H,C) |
| 145-165 м.д. | ароматические О-замещенные атомы углерода (CAr-O) |
| 165-187 м.д. | атомы углерода карбоксильных групп и их производных (CCOOH(R)) |
| 187-220 м.д. | атомы углерода кетонных и хинонных групп (CС=О) |
В ряде работ было выполнено сопоставление фрагментного состава ГВ различного происхождения. Так, на основании сопоставления результатов 13С ЯМР исследования структуры препаратов ФК дерново-подзолистых почв и природных вод показано, что последние характеризуются более высоким содержанием алифатических фрагментов, в то время как фрагментный состав ГК этих природных сред довольно близок [37, 38].
Также проводилось сопоставление гуминовых веществ торфа и дерново- подзолистых почв. Показано, что ГВ торфа характеризуются более высоким содержанием ароматических и углеводных фрагментов, нежели ГВ почв, а содержание карбоксильных и алкильных групп в случае гуминовых веществ торфа несколько ниже [39, 40].
Сравнительное исследование структуры ГК бурых углей, ФК и ГК дерново- подзолистых почв показало, что содержание -СООН групп в ГК угля ниже, чем в ФК почв, однако выше, нежели в ГК почв [38, 41]. По сравнению с ГК почв ГК угля характеризуются значительно более высокой ароматичностью, и очень низким содержанием углеводных структур.
Таким образом, данные по количественному исследованию структурных фрагментов ГВ свидетельствуют о том, что все ГВ независимо от источника происхождения обладают сходным набором основных структурных фрагментов. При этом количественное соотношение структурных фрагментов может варьировать в зависимости от источника.
1.1.4. Молекулярно-массовый состав гуминовых веществ
Все ГВ можно считать высокомолекулярными соединениями, хотя дискуссии о размерах молекулярных масс (ММ) продолжаются до последнего времени. Исторически в этом отношении выявляются несколько этапов. На ранних этапах гуминовым кислотам приписывали низкие и постоянные величины ММ. 80—90 лет назад их считали равными 1400 атомных единиц массы (а.е.м.), затем возобладало мнение, что ГВ полидисперсны, поэтому к ним неприменимы понятия ММ. После развития химии высокомолекулярных соединений и появления новой аналитической техники стали считать, что ММ фульвокислот близки к 10—15 тыс. а.е.м., а гуминовых кислот — от 20—30 тыс. до 100—150 тыс. а.е.м. В начале 80-х годов XX века было показано, что крупные частицы гуминовых кислот могут изменяться под влиянием детергентов и комплексонов, которые разрушают сложные ассоциаты молекул, снижая их средние молекулярные массы.
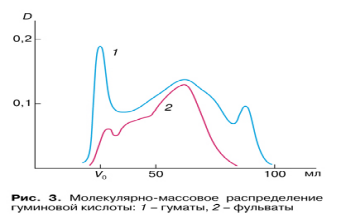
Наиболее эффективным приемом определения средних ММ и молекулярно-массового распределения (ММР) ГВ оказалась гель-фильтрация. На рис. 3 по оси абсцисс отложены объемы раствора гумата натрия, прошедшего через колонку с гелем сефа-декса G-75, а по ординате — оптические плотности соответствующих порций раствора. Площади, занимаемые отдельными максимумами в первом приближении, пропорциональны количественному со¬держанию фракций ГВ с определенными ММ. Первыми из колонки выходят фракции с наиболь¬шими ММ, их максимумы расположены ближе к началу координат. Чем дальше от начальной точки, тем меньшие ММ характерны для отдельных фракций. Усредненные величины ММ соответствуют на рис. 3 числам вблизи соответствующих максимумов. Эти данные не требуют комментариев, но необходимо обратить внимание на то, что в одном и том же препарате присутствуют одновременно молекулы с разными ММ, причем диапазон величин достаточно высок. Это одна из причин полифункциональности ГВ наряду с изменчивостью их состава, поскольку если одни молекулы ГВ по какой-либо причине не могут участвовать в химических или физиологических процессах, то всегда найдутся другие подходящие для таких процессов по размерам и свойствам.
Молекулярная масса (ММ) фундаментальная характеристика любого химического вещества, в том числе и гуминовых веществ. Молекулярные массы ГВ по разным данным составляют от 700 до 200000 Дальтон (Да) [10, 42, 43]. От размеров и конфигурации частиц ГК и ФК зависят их растворимость, способность к миграции, возможность поглощения микроорганизмами и высшими растениями [2]. Так же молекулярная масса ГВ в некоторой степени определяет их способность к связыванию ионов различных металлов. В работе [44] рассмотрена способность ГВ к связыванию кадмия. Отмечено, что фракция ГВ с молекулярной массой 1000-10000 Да связывает основную часть ионов кадмия. Авторами [44] было установлено, что именно в этой фракции энергия связи ГВ и металла на порядок выше, чем во фракциях с меньшей или большей молекулярной массой.
Известно, что ММ закономерно изменяется для ГВ разного происхождения (табл. 1.4) [22, 45]. Согласно существующим литературным данным, ГВ можно расположить в следующий ряд по возрастанию их ММ: ФК природных вод
Таблица 1.4
Молекулярные массы гуминовых веществ различного происхождения
| Образцы | Диапазон Mw, кДа |
| водные ФК | 0.3-17 |
| водные ГК и ГВ | 1-30 |
| угольные ГК | 4-7 |
| торфяные ГК | 4-22 |
| дерново-подзолистые ФК | 1-5 |
| дерново-подзолистые ГК | 100-700 |
| почвенные | 100-200 |
Наиболее распространенным методом определения молекулярно-массового распределения ГВ является гель-проникающая (эксклюзионная) хроматография (ГПХ). Сущность метода эксклюзионной хроматографии заключается в пространственном разделении молекул различных размеров с помощью пористых гелей. Молекулы, размеры которых малы по сравнению с порами геля, свободно диффундируют во всем объеме геля, а крупные молекулы в поры не проникают и остаются во внешнем объеме растворителя. Фракционирование осуществляют в колонке, заполненной макропористым сорбентом, пространство между гранулами и поры геля заполнены растворителем. Колонку калибруют по веществам с известными молекулярными массами. В качестве образцов сравнения для ГВ используют полидекстраны, полиакрилаты, полистиролсуфонаты [45].
В силу полиэлектролитного характера ГВ, в процессе их ГПХ- фракционирования возникают неэксклюзионные эффекты: сверхэксклюзии и специфической сорбции [45, 46-48]. Эффект сверхэксклюзии обусловлен электростатическим отталкиванием между полианионами ГВ и частично отрицательно заряженными участками гидрофильного геля, что ведет к уменьшению объемов удерживания и завышенным значениям ММ [45]. Специфическая сорбция возникает в результате образования гидрофобных или водородных связей между аналитом и матрицей геля. Как следствие, объем элюирования аналита возрастает, что приводит к занижению определяемого значения ММ [45, 47]. При изучении низкомолекулярных аналогов ГВ было установлено, что для всех ароматических оксикислот характерна высокая специфическая сорбция, а для всех карбоновых ароматических и алифатических кислот - эффект сверхэксклюзии [45, 48, 49]. Так как гуминовые вещества включают в себя как ионогенные функциональные группы, гидрофильные углеводные фрагменты, так и гидрофобные ароматические и алкильные фрагменты, то их поведение обусловлено комплексом описанных выше эффектов.
Для частичного подавления неэксклюзионных эффектов в элюент вводят модифицирующие агенты, например, фоновые электролиты, изменяющие ионную силу, спирты, уменьшающие диэлектрическую проницаемость элюента, и др.
Имеющиеся литературные данные по составу и строению ГВ показывают, что содержащиеся в них структурные фрагменты (карбоксилы, фенольные гидроксилы, различные серу- и азотсодержащие группы) позволяют ожидать, что ГВ обладают высоким сродством к различным органическим экотоксикантам и к ионам металлов. Кроме того, обширный набор функциональных групп открывает широкие возможности для химической модификации ГВ.
ЭЛЕКТРОННЫЕ И МОЛЕКУЛЯРНЫЕ СПЕКТРЫ.
Спектральные данные (включая спектры ЭПР и ЯМР) подтверждают сведения, полученные с помощью "мокрой" химии. Тем не менее некоторые из них нуждаются в пояснении. Электронные спектры (ультрафиолетовая и видимая области — от 220 до 750 нм) объясняют темную окраску ГВ. В этом интервале длин волн спектры ГВ имеют характер пологих, опускающихся в сторону больших длин волн, кривых, на которых практически нет никаких максимумов или минимумов. Большая часть авторов объясняет это тем, что в молекулах ГВ достаточно сильно развита цепь сопряженных двойных углеродуглеродных связей. Разрушение этой цепи при фотохимическом расщеплении приводит постепенно к потере окраски.
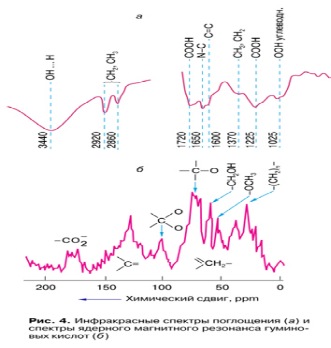
Инфракрасные спектры ГВ, как и спектры ЯМР, имеют характерный набор полос поглощения, которые могут использоваться для идентификации вещества и нахождения тех атомных групп, из которых сложены молекулы. Это хорошо видно на рис. 4.
Функции ГВ
ГВ - активируют клеточный метаболизм и регенеративные процессы. Механизм его действия заключается в повышении активности некоторых ферментов, в результате чего ускоряются окислительно – восстановительные процессы, улучшает газообмен и тканевое дыхание, подавляется интенсивность свободно-радикального окисления в тканях. Кислоты низкого молекулярного веса такие как фульвовая кислота которая может активизировать ‘'спящие''нейтроны путем интенсификации клеточного дыхания .''Проснувшись'',эти нейтрофилы способны разбудить всю иммунную систему .Получены данные ,что фульвовая кислота ,выделенная из торфа ,активно ловит свободные радикалы .
Препарат способствует репарации соединительной ткани. ГВ образуются в почвах, торфах, углях, других природных телах. Они накапливают элементы питания и энергию, участвуют в миграции катионов. Снижают негативное действие токсичных веществ, влияют на развитие организмов и тепловой баланс планеты. Они устойчивы, высокомолекулярны, полидисперсны. Содержат различные функцианальные группы, аминокислоты, полисахариды и др. [3/] Гуминовые вещества выполняют в биосфере множество функций из которых важнейшие следующие:
1. Аккумулятивная функция. Она заключается в накоплении химических элементов и энергии, необходимых живым организмам. В составе гуминовых веществ найдено от 40 до 60% С, 3-5% N, 30-40% О, а также водород, сера, фосфор, многие металлические катионы, в том числе так называемые микроэлементы. Не случайно темно-серые и черные по цвету почвы в народе всегда считали плодородными и называли, хотя и не всегда правильно, черноземами. Окраску таким почвам придают ГВ.
Гуминовые вещества отдают живым организмам необходимые им элементы питания постепенно, по мере их потребления, сохраняя тем самым необходимый запас этих элементов для последующих поколений. Этим они существенно отличаются от многих минеральных соединений, которые могут снабжать растения элементами питания, но представлены, как правило, легкорастворимыми веществами, которые быстро расходуются или вымываются из почвы. В то же время часть минеральных элементов входит в кристаллическую решетку алюмосиликатов, они недоступны живым организмам и только после разрушения минералов потребляются растениями.
Азот – важнейший элемент питания растений. Соединения азота играют большую роль в процессах фотосинтеза, обмена веществ, образования новых клеток. Основные запасы азота на Земле находятся в атмосфере. В почве его всего 3-5%. Но главным источником азота в почве является гумус.
2. Транспортная функция. Она заключается в формировании геохимических потоков минеральных и органических веществ, преимущественно в водных средах, за счет образования устойчивых, но сравнительно легкорастворимых комплексных соединений гумусовых кислот с катионами металлов или гидроксидами. Транспортная функция до некоторой степени противоречит аккумулятивной функции, поскольку их результаты прямо противоположны, но противоречивость действия обеспечивает многообразие влияния гуминовых веществ на минеральные компоненты почв и горных пород.
3. Регуляторная функция. Эта функция объединяет множество различных явлений и процессов и относится к почвам, водам и другим природным телам. В регуляторной функции гуминовых веществ можно выделить несколько главных составляющих: формирование почвенной структуры и водно-физических свойств почв; регулирование реакций ионного обмена между твердыми и жидкими фазами; влияние на кислотно-основные и окислительно-восстановительные режимы; регулирование условий питания живых организмов путем изменения растворимости минеральных компонентов; регулирование теплового режима почв и атмосферы, включая проявления парникового эффекта.
4. Протекторная функция, которая заключается в способности гуминовых веществ связывать в малоподвижные или труднодиссоциирующие соединения токсичные и радиоактивные элементы, а также соединения, негативно влияющие на экологическую ситуацию в природе, в том числе они могут инкорпорировать некоторые пестициды, углеводороды, фенолы. Защитная функция гуминовых веществ настолько велика, что богатые ими почвы могут полностью предотвратить поступление в грунтовые воды ионов свинца и других токсичных веществ.
5. Физиологическая функция. Многими исследователями было установлено, что различные гуминовые вещества, особенно гуминовые кислоты и их соли, могут стимулировать прорастание семян, активизировать дыхание растений, повышать продуктивность крупного рогатого скота, птицы. Более того, было показано, что некоторые препараты гуминовых веществ сдерживают развитие злокачественных опухолей, повышают устойчивость организмов к различного рода воспалительным процессам.[2/]
Список цитируемой литературы
1. Тарновская Л.И., Маслов С.Г. Изменение химического состава гуминовых кислот в процессе термолиза торфа // Химия твердого топлива. - 1994. - № 4-5. - С. 33-39.
2- Гуминовые удобрения. Теория и практика их применения / Отв. ред. В.П. Попов. – Киев: Гос.изд. с/х лит., 1962. – 649с.
3/ http://biotehnologya.narod.ru/Pages/1_3.html
1. Орлов Д.С. Химия почв. М.: Изд-во МГУ. 1992. 259 с.
2. Орлов Д.С. Свойства и функции гуминовых веществ. В сб.: Гуминовые вещества в биосфере. М.: Наука. 1993. 298 с.
3. Линник П.Н., Набиванец Б.И. Формы миграции металлов в пресных поверхностных водах. Гидрометеоиздат. Л. 1986. 268 с.
4. Орлов Д. С. Гумусовые кислоты почв. М.: Изд-во МГУ. 1974. 287 с.
5. Драгунов С.С. Методы исследования гумусовых веществ. Труды почв. инст. им.
Докучаева. 1951. Т. 38. С. 86-98.
6. Ковалевский Д. В., Пермин А. Б., Перминова И. В., Петросян В. С.. Выбор условий регистрации количественных 13С ЯМР-спектров гумусовых кислот. // Вестн. МГУ. Сер.2. Химия. 2000.Т.41.№1. С. 39-43.
7. Ковалевский Д.В. Исследование структуры гумусовых кислот методами спектроскопии ЯМР 1Н и 13С. Дисс. канд.хим.наук. Москва. МГУ. 1998. 157 с.
8. Данченко Н.Н. Функциональный состав гумусовых кислот: определение и взаимосвязь с реакционной способностью. Дисс. канд. хим. наук. Москва. МГУ.
1997 г. 135 с.
9. Perminova I.V., Frimmel F.H., Kudryavtsev A.V., Kulikova N.A., Abbt-Braun G., Hesse S., Petrosyan S. Molecular weight characteristics of humic substances from different environments as determined by size exclusion chromatography and their statistical evaluation.// Environ. Sci. Technol. 2003. V 37. P. 2477-2481.
10. Славинская Г.В., Селеменев В.Ф. Фульвокислоты природных вод. Воронеж: Б.и.
2001. 156 с.
11. Перминова И.В. Анализ, классификация и прогноз свойств гумусовых кислот.
Дисс. док. хим. наук, Москва. МГУ. 2000. 359 с.
12. Кноп А., Шейб В. Фенольные смолы и материалы на их основе. (Пер. с англ. А.
М. Василенко, Г. М. Восканянца: Под ред. Ф.А.Шутова). М.: Химия. 1983. 280 с.
13. Серенсон У., Кемпбел Т. Препаративные методы химии полимеров.(Пер. с англ.
Под редакцией С.Р. Рафикова). М.: Изд-во иностранной литературы. 1963. 400 с.
14. Браун Д., Шердрон Г. Практическое руководство по синтезу и исследованию свойств полимеров. (Пер. с нем. Под ред. В. П. Зубова.) М.: Химия. 1976. 311 с.
58. Arsenie I., Boren H., Allard B. Determination of the carboxylic content in. humic substances by methylation. //Sci. Total Environ. 1992. V. 116. P. 213-220.
59. Mikita M.A., Steelink C., Wershaw R.L. Carbon-13 enriched nuclear magnetic resonance method for the determination of hydroxyl functionality of humic substances.
//Anal. Chem. 1981. V. 53. No. 11. P. 1715-1717.
60. Almendros G., Dorado J. Molecular characteristics related to the biodegradability of humic acid preparations. // European Journal of Soil Science. 1999. V.50. P. 227-236.
68. Сиггиа С., Ханна Дж. Г. Количественный органический анализ по функциональным группам. (Пер.с англ., под ред. А.П. Сергеева). М.: Химия. 1983. C. 132-135.
69. Almendros G. Effects of different chemical modifications on peat humic acid and their bearing on some agrobiological characteristics of soils. // Commun. Soil. Sci. Plant Anal. 1994. V. 25. P. 2711-2736.
70. Herzog, H., Burba, P., Buddrus J. Quantification of hydroxylic groups in a river humic substance by Si(29)-NMR. // Anal.Chem.1996. V. 354. No. 3. P. 375-377.
72. Dec J., Haider K., Shaffer A. Use of a silylation procedure and 13C-NMR spectroscopy to characterize bound and sequestered residues of cyprodinil in soil. // Environ. Sci. Technol. 1997. V. 31. P. 2991-2997.
73. Monsef-Mirzai P., McWhinnie W.R., Perry M.C. Measurement of OH-groups in coals of different rank using microwave methodology, and the development of quantitative solid state n.m.r. methods for in situ analysis. // Fuel. 1995. V.74. №5. P. 674-683.
79. Попова О.В. Научные основы электрохимического модифицирования лигнинов.
Дисс. док. хим. наук. Саратов. РГБ ОД. 2006. 291 c.
80. Передникова З.М., Румянцева З.А., Гарцман Б.Б. Изучение химического состава и строения фюзинитовых бурых углей по продуктам их озонирования. // ХТТ. 1992. Т.1. С. 36-43.
81. Платонов В.В., Клявина О.А., Воль-Эпштейн А.Б., Ивлева Л.Н., Таболенко Н.В., Окушко В.Д. Озонирование нейтральных кислородосодержащих соединений первичной каменноугольной смолы.// ХТТ. 1987. T.1. C. 88-91.
83. Жамбал Д. Состав и структурные особенности сульфогуминовых кислот. // ХТТ. 1991. №2. С.70-72.
91. Prado A.G.S., Sales J.A.A., Airoldi C. The increased thermal stability associated with humic acid anchored onto silica gel. // Journal of Therm. Anal. And Calorim. 2002. V.
70.P. 191-197.
93. Klavins M., Eglite L. Immobilization of humic substances. // Coll. And. Surf. A.
2002.V. 203. P. 47-54.
94. Andre C., Thomassin M., Berthelot A. A stepwise stoichiometric representation to confirm the dependence of pesticide/humic acid interactions on salt concentration and to test the performance of a silica bonded humic acid column. // Anal. Chem. 2006. V.78. P.873-882.
97. Варшал Г.М., Кощеева И.Я. О механизме сорбции ртути (II) гуминовыми кислотами. //Почвовед. 1998. №9б. C. 1071-1078.
98. Варшалл Г.М., Велюханова Т.К. Геохимическая роль гумусовых кислот в миграции элементов. Гуминовые вещества в биосфере. М.: Наука, 1993. 234 c.
112. Евдокимова Г.А., Морозова Н.М. Миграция тяжелых металлов из почвы в сельскохозяйственные культуры. // В сб.: Тяжелые металлы в окружающей среде и охрана природы. Мат. II Всесоюзн. конф., 28-30 дек. 1987 г., ч. II, М., 1988, С.
204-209.
113. Корнилович Б.Ю., Пшинко Г.Н., Ковальчук И.А. Влияние фульвокислот на взаимодействие U (VI) с глинистыми компонентами почв. // Радиохимия. 2001. Т.
43. № 5. C. 464-467.
114. Кабата-Пендиас А., Пендиас Х. Микроэлементы в почвах и растениях. М. 1989.
439 с.
188. Лисичкин Г.В. Модифицированные кремнеземы в сорбции, катализе и хроматографии. М.: Химия. 1986. 237с.
215. Posner G.H., Rogers D.Z. Organic reactions at alumina surfaces. Mild and selective opening of arene and related oxides by weak oxygen and nitrogen nucleophiles. // J. Am. Chem. Soc. 1977. V.99. P. 8214-8218.
216. Бергер В., Беккер Х., Беккерт Р. Органикум 2 т. (Пер. с нем. Н.А.Беликовой,
Г.В.Гришиной, С.В.Грюнера). Изд. Мир. 1992.
228. Жилин Д.М. Исследование реакционной способности и детоксицирующих свойств гумусовых кислот по отношению к соединениям ртути (II). Дисс. канд. хим. наук. Москва. МГУ. 1998. 187 c.












