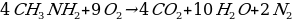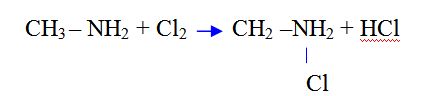Тема. Амины. Строение молекул аминов. Номенклатура аминов. Физические свойства аминов. Химические свойства алифатических аминов на примере метиламина: реакция с водой, галогеноводородами, горение аминов.
Цель: - сформировать понятие об аминогруппе, аминах как органических основаниях.
Тип урока: изучение нового материала
Ход урока:
Организационный момент.
Актуализация знаний
Беседа по вопросам:
Перечислите элементы-органогены. (Углерод, водород, кислород, азот)
На какие группы делят органические вещества по составу? (Углеводороды, кислородсодержащие, азотсодержащие соединения)
Вспомните функциональные группы, характерные для органических веществ. (Гидроксильная, альдегидная, карбоксильная, нитрогруппа – нитроглицерин, нитроцеллюлоза)
Как классифицируют атомы углерода (в зависимости от количества атомов углерода, с которыми они связаны)? (Первичный, вторичный, третичный, четвертичный)
Встречались ли мы с вами с азотсодержащими органическими соединениями? Приведите примеры.
В чем отличие кислотных и основных свойств?
Кислотные свойства – отщепление Н+
Основные свойства – присоединение Н+
Изучение нового материала.
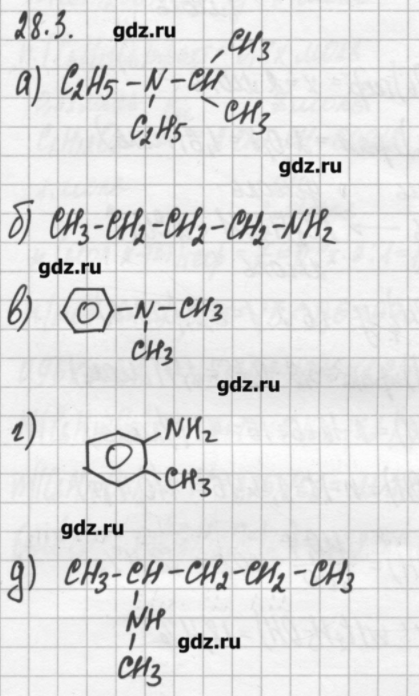
Амины – производные углеводородов, в которых атом водорода замещен на аминогруппу –NH2. С другой стороны, их можно представить как продукты замещения атомов водорода в молекуле аммиака на органические радикалы. В зависимости от числа замещенных атомов различают первичные, например метиламин CH3NH2, вторичные, такие, как диэтиламин(C2H5)2NH, и третичные амины, примером которых может быть диметилэтиламин(CH3)2(C2H5)N. Из последнего примера видно, что присоединенные к атому азота группы могут быть неодинаковыми.
Сходство аминов с аммиаком не формальное. Эти вещества имеют схожие свойства, в частности и аммиак, и амины проявляют основные свойства (слабые основания).
Названия аминов производят от названия радикалов, входящих в молекулу, с добавлением окончания -амин:
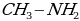 метиламин,
метиламин,
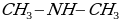 диметиламин,
диметиламин,
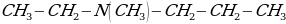 метилэтилпропиламин
метилэтилпропиламин
Для аминов можно выделить 3 типа изомерии:
1.Изомерия углеродного скелета:
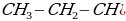 изобутиламин
изобутиламин
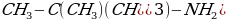 третбутиламин
третбутиламин
2.Изомерия положения функциональной группы:
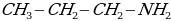 пропиламин-1
пропиламин-1
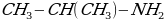 пропиламин-2
пропиламин-2
3.Изомерия между типами аминов:
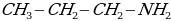 первичный амин
первичный амин
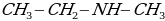 вторичный амин
вторичный амин
По физическим свойствам:
Низшие амины при нормальных условиях – газы, имеющие запах аммиака
Средние – жидкости со слабым запахом аммиака
Высшие – твердые вещества без запаха
Метиламин, диметиламин и триметиламин — газообразные вещества, с запахом аммиака, хорошо растворяются в воде, так как их молекулы образуют водородные связи с молекулами воды. Средние члены алифатического ряда – жидкости со слабым запахом тухлой рыбы, с постепенно повышающейся температурой кипения. Высшие амины (начиная с С16Н35N — твердые нерастворимые вещества, не имеющие запаха. Ароматические амины – бесцветные высококипящие жидкости или твердые вещества, практически нерастворимые в воде. Связь N–H является полярной, поэтому первичные и вторичные амины образуют межмолекулярные водородные связи (несколько более слабые, чем Н-связи с участием группы О–Н).Это объясняет относительно высокую температуру кипения аминов по сравнению с неполярными соединениями со сходной молекулярной массой.
Анилин (фениламин) С6H5NH2 – важнейший из ароматических аминов:
Анилин представляет собой бесцветную маслянистую жидкость с характерным запахом (т. кип. 184 °С, т. пл. – 6 °С). На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит.
Химические свойства
1.взаимодействие с кислотами:
Так как амины основания, то они, как и аммиак, вступают в реакцию с кислотами. При этом образуются соли.
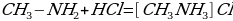 хлорид метиламмония
хлорид метиламмония
2. взаимодействие с водой:
При взаимодействии с водой амины, как и аммиак, присоединяют протон (ион водорода Н+) по месту свободной неподеленной пары атома азота, что ведет к накоплению гидроксид-ионов в растворе. Поэтому растворы аминов проявляют щелочную реакцию. Индикаторы изменяют свою окраску в растворах аминов следующим образом: лакмус – синий, метилоранж – желтый, фенолфталеин – малиновый.
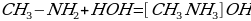 гидроксид метиаммония
гидроксид метиаммония
3.Амины горят на воздухе с образованием углекислого газа и, воды и азота:
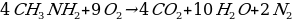
4.Реакция галогенирования:
Амины, как и алканы, вступают в реакции замещения с галогенами
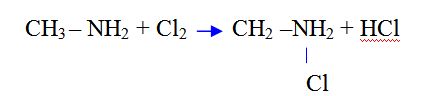
Основные свойства в ряду метиламин →аммиак→анилин ослабевают.
Закрепление знаний

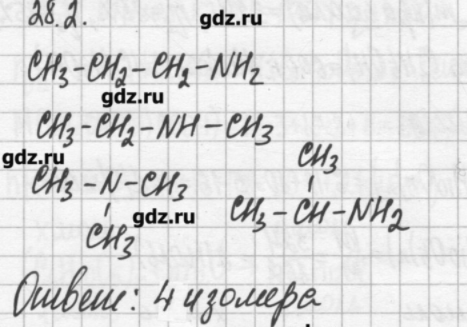


Домашнее задание







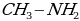 метиламин,
метиламин,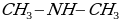 диметиламин,
диметиламин, 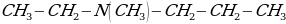 метилэтилпропиламин
метилэтилпропиламин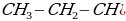 изобутиламин
изобутиламин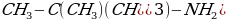 третбутиламин
третбутиламин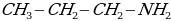 пропиламин-1
пропиламин-1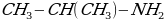 пропиламин-2
пропиламин-2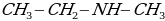 вторичный амин
вторичный амин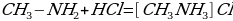 хлорид метиламмония
хлорид метиламмония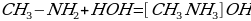 гидроксид метиаммония
гидроксид метиаммония